2025年には超高齢社会になると予測された台湾でも、ポールウォーキングは普及し出しています!
関連学術ニュースは、「積極的に頭を使うことによって認知機能の低下が遅くなるだけではなく、認知機能がむしろ向上し、認知症の発症が遅くなる!」という実証研究報告の論文紹介と、岐阜大学下畑先生からの最新医学情報です。
特別企画『AIに訊く』では、新たにスタートさせる「連載シリーズ:切り替えの物語 — AIとの対話から生まれた統合理論」のイントロ・第1回をお届けします(AIとの共作論文は当サイトのトピックスに順次掲載してゆきます)。
1.2026年4月の活動状況
・スマイルチームさんの投稿
 20260403 スマイルチーム上鶴間 天気予報によると今日が最後のお花見日和、、、らしい日に 参加下さった皆さん、ありがとうございました☺️ 体の細かいところを理解しながらのエクササイズ。 かなりの脳トレになるリズムエクササイズ。 体の隅々までのストレッチ。 時間内たっぷりと頭も体も動かすことができました。 お疲れ様でした😊 #スマイルチーム上鶴間 #相模原市南区 #上鶴間公民館
20260403 スマイルチーム上鶴間 天気予報によると今日が最後のお花見日和、、、らしい日に 参加下さった皆さん、ありがとうございました☺️ 体の細かいところを理解しながらのエクササイズ。 かなりの脳トレになるリズムエクササイズ。 体の隅々までのストレッチ。 時間内たっぷりと頭も体も動かすことができました。 お疲れ様でした😊 #スマイルチーム上鶴間 #相模原市南区 #上鶴間公民館
・台灣健走杖運動推廣協會さんの投稿
 🎬✨ 會員大會圓滿落幕|精彩瞬間回顧 2026 台灣健走杖運動推廣協會 第二屆第一次會員大會,圓滿完成!🎉 從報到的熱絡問候、 會議中的專注與交流, 到戶外健走杖運動會的歡笑與活力, 每一個畫面,都是我們一起走過的美好瞬間。💚 因為有你們, 這不只是一場活動, 而是一段彼此連結的旅程。 謝謝每一位到場的夥伴, 下一段路,我們繼續一起走!🚶♀️🚶♂️ #台灣健走杖運動推廣協會 #雙杖在手健康跟著走
🎬✨ 會員大會圓滿落幕|精彩瞬間回顧 2026 台灣健走杖運動推廣協會 第二屆第一次會員大會,圓滿完成!🎉 從報到的熱絡問候、 會議中的專注與交流, 到戶外健走杖運動會的歡笑與活力, 每一個畫面,都是我們一起走過的美好瞬間。💚 因為有你們, 這不只是一場活動, 而是一段彼此連結的旅程。 謝謝每一位到場的夥伴, 下一段路,我們繼續一起走!🚶♀️🚶♂️ #台灣健走杖運動推廣協會 #雙杖在手健康跟著走
・田村 芙美子さんの投稿
 昨夜 あの渋谷のスクランブル交差点で🔥🔥🔥 渋谷区介護予防ポールウォーキング教室新年度1学期が始まりました。抽選をクリアした15名の方々。このクラスを申し込まれた理由は・・ ・姿勢を改善したい ・脊柱管狭窄症で片足が痺れて歩きにくい ・人工股関節をいれたので歩くのが不安 ・以前教室を覗いたら楽しそうだった ・T字杖を使用しているが身体が傾くようで不安 etc. 皆さんの不安を安心に! 筋バランスを整え姿勢良く転ばないよう安定して歩けるように 愉しく運動しましょう。 鎌倉段葛は🌸が満開です。
昨夜 あの渋谷のスクランブル交差点で🔥🔥🔥 渋谷区介護予防ポールウォーキング教室新年度1学期が始まりました。抽選をクリアした15名の方々。このクラスを申し込まれた理由は・・ ・姿勢を改善したい ・脊柱管狭窄症で片足が痺れて歩きにくい ・人工股関節をいれたので歩くのが不安 ・以前教室を覗いたら楽しそうだった ・T字杖を使用しているが身体が傾くようで不安 etc. 皆さんの不安を安心に! 筋バランスを整え姿勢良く転ばないよう安定して歩けるように 愉しく運動しましょう。 鎌倉段葛は🌸が満開です。
・中村 理さんの投稿
 佐久ポールウォーキング協会より 4/5(日) 本日2026年度PW歩き始め〜❗️ 定例会場/駒場公園に60名越えの参加者を迎え、少し汗ばむ公園〜牧場の散策が出来ました。 初心者🔰6人の体験コースや健脚〜ユックリコースの3コースでの歩き染め。来週は桜満開?の別な公園散策です❗️ PS:新MC pro/遠藤パパ〜 この3月誕生で資格授与もありました〜❗️ 当協会発展の為ご活躍を期待しま〜す⁉️
佐久ポールウォーキング協会より 4/5(日) 本日2026年度PW歩き始め〜❗️ 定例会場/駒場公園に60名越えの参加者を迎え、少し汗ばむ公園〜牧場の散策が出来ました。 初心者🔰6人の体験コースや健脚〜ユックリコースの3コースでの歩き染め。来週は桜満開?の別な公園散策です❗️ PS:新MC pro/遠藤パパ〜 この3月誕生で資格授与もありました〜❗️ 当協会発展の為ご活躍を期待しま〜す⁉️
・Masako Shinchiさんの投稿
 ☘️佐久といえば、この風景☘️ 雪が消えた浅間山、桜の蕾がうっすら赤くなり始めた駒場公園、そしてポールを持って歩く人たち 家から出てみれば、この風景のおかげで、うつむいてはいられない。
☘️佐久といえば、この風景☘️ 雪が消えた浅間山、桜の蕾がうっすら赤くなり始めた駒場公園、そしてポールを持って歩く人たち 家から出てみれば、この風景のおかげで、うつむいてはいられない。
・遠藤 恵子さんの投稿
 【本日の介護予防運動教室にて】 体操終了後、 初めてご参加くださった方が 涙を浮かべながら声をかけてくださいました。 「先生の体操、とっても良かったです。 お話も精神的にも本当に良くて… 良いお話が聞けて嬉しかったです。 ありがとうございました。」 そう言っていただけて、 とても嬉しくて、励みになりました。 私自身の経験も交えながら、 新年度はじまったばかりなのでお話多め セロトニンについてや脳トレ… 「この運動は何のために必要なのか」 をお伝えしました。 ただ身体を動かすだけでなく、 心にも届く時間になっていたら嬉しいです。 今日も素敵な出会いに感謝です✨ さっ 次の講座へ移動🚙💨
【本日の介護予防運動教室にて】 体操終了後、 初めてご参加くださった方が 涙を浮かべながら声をかけてくださいました。 「先生の体操、とっても良かったです。 お話も精神的にも本当に良くて… 良いお話が聞けて嬉しかったです。 ありがとうございました。」 そう言っていただけて、 とても嬉しくて、励みになりました。 私自身の経験も交えながら、 新年度はじまったばかりなのでお話多め セロトニンについてや脳トレ… 「この運動は何のために必要なのか」 をお伝えしました。 ただ身体を動かすだけでなく、 心にも届く時間になっていたら嬉しいです。 今日も素敵な出会いに感謝です✨ さっ 次の講座へ移動🚙💨
・校條 諭さんの投稿
 最高気温27度予報にもかかわらず快適ポール歩き 4月の気まポ(気ままにポール歩き)は、当初予定していた石神井川沿いを歩くのをやめて、主として石神井公園の中を歩くコースに急遽変更しました。川沿いは緑が少ないので。 公園内は木陰が多く、湿度も低かったので、とても気持ちのよいウォーキングでした。2つの池を一周すると、次々に開ける視界がさまざまに変化するので飽きません。 途中、少しだけ公園から離れて、三宝寺という寺に寄りました。ここには四国八十八箇所をインスタントにお遍路できる場所があります。
最高気温27度予報にもかかわらず快適ポール歩き 4月の気まポ(気ままにポール歩き)は、当初予定していた石神井川沿いを歩くのをやめて、主として石神井公園の中を歩くコースに急遽変更しました。川沿いは緑が少ないので。 公園内は木陰が多く、湿度も低かったので、とても気持ちのよいウォーキングでした。2つの池を一周すると、次々に開ける視界がさまざまに変化するので飽きません。 途中、少しだけ公園から離れて、三宝寺という寺に寄りました。ここには四国八十八箇所をインスタントにお遍路できる場所があります。
・水間 孝之さんの投稿
 中台科術大学 許秀貞先生のチェアエクササイズ 楽しい❣️
中台科術大学 許秀貞先生のチェアエクササイズ 楽しい❣️
・Masako Shinchiさんの投稿
 〜ウォーキングポールを相棒に仲間と巡る小さな旅〜 ぽる旅 第4弾🌷 霞ヶ浦総合公園で霞ヶ浦のキラキラ光る湖面を眺めつつ、チューリップに元気をもらう旅、です! 常磐線土浦駅下車、市内周遊バスで20分 シンボルの大きな風車の前には色鮮やかなチューリップが。 このチューリップは誰のものなんですかねー?と、昭和14年生まれFさんの渾身の振りに誰も気付けず、30秒後に「オランダ〜‼️」😄遅っ。 今日は土浦市在住の関コーチが駆けつけてくださいました。股関節の手術を終えリハビリ中の関さんから、日頃歩いたりストレッチ、筋トレをしていたことでリハビリがスムーズに進んでいるというお話が。みんな真剣に聞き入りました。 ポールで歩くことでこうした交流ができるのは本当に嬉しいです😊また一緒にに歩きましょうと約束をしました。 花も光も人にも力をもらいました。さぁ気持ちよい季節は歩きましょう!
〜ウォーキングポールを相棒に仲間と巡る小さな旅〜 ぽる旅 第4弾🌷 霞ヶ浦総合公園で霞ヶ浦のキラキラ光る湖面を眺めつつ、チューリップに元気をもらう旅、です! 常磐線土浦駅下車、市内周遊バスで20分 シンボルの大きな風車の前には色鮮やかなチューリップが。 このチューリップは誰のものなんですかねー?と、昭和14年生まれFさんの渾身の振りに誰も気付けず、30秒後に「オランダ〜‼️」😄遅っ。 今日は土浦市在住の関コーチが駆けつけてくださいました。股関節の手術を終えリハビリ中の関さんから、日頃歩いたりストレッチ、筋トレをしていたことでリハビリがスムーズに進んでいるというお話が。みんな真剣に聞き入りました。 ポールで歩くことでこうした交流ができるのは本当に嬉しいです😊また一緒にに歩きましょうと約束をしました。 花も光も人にも力をもらいました。さぁ気持ちよい季節は歩きましょう!
・中村 理さんの投稿
 佐久ポールウォーキング協会より PW散策年度初め〜❗️ 桜🌸満開の〜さくラさく小径公園〜をポールウォークで闊歩。 桜見頃を測った参加者70名越えの皆さん、ドンピシャの桜🌸🌸🌸〜 皆さん日頃の行い良好にての結果、ワンコ連れやランドセルnew〜newのピカピカの小学生写真撮りやら楽しみ満喫の公園PW3〜5kmの散策でした‼️
佐久ポールウォーキング協会より PW散策年度初め〜❗️ 桜🌸満開の〜さくラさく小径公園〜をポールウォークで闊歩。 桜見頃を測った参加者70名越えの皆さん、ドンピシャの桜🌸🌸🌸〜 皆さん日頃の行い良好にての結果、ワンコ連れやランドセルnew〜newのピカピカの小学生写真撮りやら楽しみ満喫の公園PW3〜5kmの散策でした‼️
・水間 孝之さんの投稿
 台湾ポールウォーキング協会設立4年目に入りました。会員コーチ75名になり始めての台湾におけるスキルアップ研修会を開催‼️ 気温30度日本からの参加者はかなり😥厳しいなか、台湾の皆さん元気に研修会完了しました。 ありがとうございました😊
台湾ポールウォーキング協会設立4年目に入りました。会員コーチ75名になり始めての台湾におけるスキルアップ研修会を開催‼️ 気温30度日本からの参加者はかなり😥厳しいなか、台湾の皆さん元気に研修会完了しました。 ありがとうございました😊
・台灣健走杖運動推廣協會さんの投稿
 2026年04月12日【日本健走杖健走初階教練(BC)培訓課程】圓滿結束! 這次也是協會開辦課程三年以來,首次有日本健走杖健走協會(NPWA)專業教練來台共同參與教練培訓課程!日本協會肯定我們在健走杖運動上的努力成果,也非常開心台灣學員的優秀表現,以及學習上的熱誠與積極。初階教練(BC)是進入日式健走的敲門磚,而進階教練(AC)則是讓我們能帶領更多人一起走出健康的專業通行認證。接下來在五月,即將開啟的進階教練培訓課程,提供更深入的專業訓練,期待更多人一同加入推動全齡健康的健走杖運動!❤️
2026年04月12日【日本健走杖健走初階教練(BC)培訓課程】圓滿結束! 這次也是協會開辦課程三年以來,首次有日本健走杖健走協會(NPWA)專業教練來台共同參與教練培訓課程!日本協會肯定我們在健走杖運動上的努力成果,也非常開心台灣學員的優秀表現,以及學習上的熱誠與積極。初階教練(BC)是進入日式健走的敲門磚,而進階教練(AC)則是讓我們能帶領更多人一起走出健康的專業通行認證。接下來在五月,即將開啟的進階教練培訓課程,提供更深入的專業訓練,期待更多人一同加入推動全齡健康的健走杖運動!❤️
・台灣健走杖運動推廣協會さんの投稿
 三年前的今天(2023/4/13),是我們重要的起點。我們與日本健走杖健走協會(NPWA)正式締結合作協議,取得授權,在台灣展開「日式健走杖健走」的推廣任務。從那一天起,一顆種子悄悄落地,開始在台灣生根發芽。而在三年前,4/14~4/16日這三天,日本專業教練來台的研習會後,台灣也有13位日本健走杖專業教練(Master Coach)取得認證。日本和台灣都面臨人口老化問題。健走杖健走,不僅僅是一項運動,從預防衰弱、降低運動傷害與跌倒風險,到透過穩定支撐改善姿態與體態,進而運用健走杖的輔助同時鍛鍊上半身與下半身肌肉,都一再讓我們感受健走杖運動帶來的價值與影響。三年來,我們持續努力、穩健步伐前進。 未來,也將繼續把這份來自日本的專業與理念,在台灣深耕、茁壯。 台灣、日本,一起加油!! 讓更多人因為「走」,而更健康、更幸福❤️
三年前的今天(2023/4/13),是我們重要的起點。我們與日本健走杖健走協會(NPWA)正式締結合作協議,取得授權,在台灣展開「日式健走杖健走」的推廣任務。從那一天起,一顆種子悄悄落地,開始在台灣生根發芽。而在三年前,4/14~4/16日這三天,日本專業教練來台的研習會後,台灣也有13位日本健走杖專業教練(Master Coach)取得認證。日本和台灣都面臨人口老化問題。健走杖健走,不僅僅是一項運動,從預防衰弱、降低運動傷害與跌倒風險,到透過穩定支撐改善姿態與體態,進而運用健走杖的輔助同時鍛鍊上半身與下半身肌肉,都一再讓我們感受健走杖運動帶來的價值與影響。三年來,我們持續努力、穩健步伐前進。 未來,也將繼續把這份來自日本的專業與理念,在台灣深耕、茁壯。 台灣、日本,一起加油!! 讓更多人因為「走」,而更健康、更幸福❤️
・台灣健走杖運動推廣協會さんの投稿
 🎬✨ 2026 教練提升課程|Skill up 花絮回顧 這一天,我們用更專注的步伐, 一起走向更專業的自己。🚶♀️🚶♂️ 從開場到課程說明、示範教學、分組演練, 每一個環節都看見大家的投入與成長。 站在前面教學的那一刻, 不只是技巧的展現,更是對「教練身份」的理解與轉變。 流流教學時的專注、 學員問題探討時的交流與回饋, 彼此觀察、修正、再進步—— 這正是教練培訓最珍貴的地方。💡 這次特別的是, 日本專業教練也來到台灣,一同參與這場課程。🇯🇵🤝🇹🇼 跨越語言與文化, 我們用相同的步伐與理念彼此交流, 讓健走杖運動的專業更加紮實,也更加有力量。 三年來, 我們一步一步,穩穩地走、持續地做。 從推廣、教學到培訓, 每一段路,都是累積。 未來, 我們也將繼續把這份來自日本的專業與理念, 在台灣深耕、茁壯。🌱 台灣、日本,一起加油!!💪 讓更多人因為「走」, 而更健康、更幸福 ❤️ ⸻ 📸 這些花絮,不只是紀錄, 更是我們一起努力過的證明。 💚 雙杖在手,健康跟著走
🎬✨ 2026 教練提升課程|Skill up 花絮回顧 這一天,我們用更專注的步伐, 一起走向更專業的自己。🚶♀️🚶♂️ 從開場到課程說明、示範教學、分組演練, 每一個環節都看見大家的投入與成長。 站在前面教學的那一刻, 不只是技巧的展現,更是對「教練身份」的理解與轉變。 流流教學時的專注、 學員問題探討時的交流與回饋, 彼此觀察、修正、再進步—— 這正是教練培訓最珍貴的地方。💡 這次特別的是, 日本專業教練也來到台灣,一同參與這場課程。🇯🇵🤝🇹🇼 跨越語言與文化, 我們用相同的步伐與理念彼此交流, 讓健走杖運動的專業更加紮實,也更加有力量。 三年來, 我們一步一步,穩穩地走、持續地做。 從推廣、教學到培訓, 每一段路,都是累積。 未來, 我們也將繼續把這份來自日本的專業與理念, 在台灣深耕、茁壯。🌱 台灣、日本,一起加油!!💪 讓更多人因為「走」, 而更健康、更幸福 ❤️ ⸻ 📸 這些花絮,不只是紀錄, 更是我們一起努力過的證明。 💚 雙杖在手,健康跟著走
・水間 孝之さんの投稿
 台湾ポールウォーキング協会BC資格取得セミナー7名の受講者、講師3名、スタッフ2名で開催。 実技研修、座学、筆記試験、実技試験7時間! 充実した時間でした。 皆さんお疲れ様です。 大変良好です‼️
台湾ポールウォーキング協会BC資格取得セミナー7名の受講者、講師3名、スタッフ2名で開催。 実技研修、座学、筆記試験、実技試験7時間! 充実した時間でした。 皆さんお疲れ様です。 大変良好です‼️
・田村 芙美子さんの投稿
 今日は、駒沢のwalking hut 2とチャッキ~の池上グループの16名が東京から遥々鎌倉ポール歩きにお出掛けくださいました。朝10時から夕方4時までのロングウォークになりました。観光客の少ない大町から材木座の寺院~材木座海岸~由比ヶ浜~扇が谷を歩き、小町通りで解散となりましたが 道中の絶え間のないお喋りオーラルトレーニングには参りました😙😗 目の前に拡がる波がキラリと光る砂浜でポールでゲーム三昧は身体中が若返り気持ちが躍りました。
今日は、駒沢のwalking hut 2とチャッキ~の池上グループの16名が東京から遥々鎌倉ポール歩きにお出掛けくださいました。朝10時から夕方4時までのロングウォークになりました。観光客の少ない大町から材木座の寺院~材木座海岸~由比ヶ浜~扇が谷を歩き、小町通りで解散となりましたが 道中の絶え間のないお喋りオーラルトレーニングには参りました😙😗 目の前に拡がる波がキラリと光る砂浜でポールでゲーム三昧は身体中が若返り気持ちが躍りました。
・堀 和夫さんの投稿
 河川環境楽園オアシスパーク 新年度ポールウォーキング教室始まりました。 出だしから雨ですので室内でポールエクササイズ。 楽しく身体動かします。
河川環境楽園オアシスパーク 新年度ポールウォーキング教室始まりました。 出だしから雨ですので室内でポールエクササイズ。 楽しく身体動かします。
・田村 芙美子さんの投稿
 100歩速歩ごとにゲームタイム
100歩速歩ごとにゲームタイム
・佐藤 ヒロ子さんの投稿
 シニアポールウォーキング 2026/4/20 参加する会員も増えて 講堂が狭くなりました 良い季節なので 外回りグループを再開! 喜んで飛んで行きます〜〜 講堂グループは足元が安心。 鏡でFormがチェックできる のも魅力です。 思い思いに分かれて 疲れたら休憩。 程よい疲労を心得ているのは シニアメンバーならばこそです 素晴らしいなあ〜〜 #船橋ウォーキングソサイエティ #ノルディックウオーク #ポールウォーキング #コグニサイズ #ポールdeダンス #しっかり歩きで免役力アップ
シニアポールウォーキング 2026/4/20 参加する会員も増えて 講堂が狭くなりました 良い季節なので 外回りグループを再開! 喜んで飛んで行きます〜〜 講堂グループは足元が安心。 鏡でFormがチェックできる のも魅力です。 思い思いに分かれて 疲れたら休憩。 程よい疲労を心得ているのは シニアメンバーならばこそです 素晴らしいなあ〜〜 #船橋ウォーキングソサイエティ #ノルディックウオーク #ポールウォーキング #コグニサイズ #ポールdeダンス #しっかり歩きで免役力アップ
・日本ポールウォーキング協会 npwaさんの投稿
 4月19日にスキルアップ研修会東京会場を実施しました。 参加者21名の内、MCProが4名参加されたため、きめ細やかなフォローや意見交換が行われ、非常にレベルの高いスキルアップ研修会になりました。 次回は7月5日(日)初の関西地区のスキルアップ研修会となります。多くの西日本地区のコーチのお申込みをお待ちしております。
4月19日にスキルアップ研修会東京会場を実施しました。 参加者21名の内、MCProが4名参加されたため、きめ細やかなフォローや意見交換が行われ、非常にレベルの高いスキルアップ研修会になりました。 次回は7月5日(日)初の関西地区のスキルアップ研修会となります。多くの西日本地区のコーチのお申込みをお待ちしております。
・佐藤 ヒロ子さんの投稿
 【美・姿勢ウォーキング初参加】 4月から新体制でスタート。 2026/4/21 土曜「ポールを使うウォーキング」から火曜日のポールを使わないウォーキングへ移った会員。 ウォーミングアップで 本人達も意外な気づき 「あれれ〜 ポールがないとふらつくわ」 そう、ポールあると無いとでは 大違い。 「4月は歩きの基本」 ウォーキングも両方経験するとより深く新鮮だったようです。 #船橋ウォーキングソサイエティ #良い歩きはよい姿勢から
【美・姿勢ウォーキング初参加】 4月から新体制でスタート。 2026/4/21 土曜「ポールを使うウォーキング」から火曜日のポールを使わないウォーキングへ移った会員。 ウォーミングアップで 本人達も意外な気づき 「あれれ〜 ポールがないとふらつくわ」 そう、ポールあると無いとでは 大違い。 「4月は歩きの基本」 ウォーキングも両方経験するとより深く新鮮だったようです。 #船橋ウォーキングソサイエティ #良い歩きはよい姿勢から
・田村 芙美子さんの投稿
 逗子PWクラブの日。朝はひんやり。家を出たところでご近所さんとバッタリ。踏切りまでおしゃべりして私は駅へ、彼女は教会へ。「辞め時」について話していて中断。 JRは今日も上下線が遅延。それでも時間までに到着し、ほっ。駅までは送迎車。 ウォーミングアップの公園の向いは今年も見事な藤! 最近裏山に猪が4頭出たそうです。クワバラクワバラ 放課後(?) 駅近くの神武寺へ。別のサークルのための下見です。特養せせらぎの前庭に数えきれないほどの大きな鯉のぼりが空を隠していました。
逗子PWクラブの日。朝はひんやり。家を出たところでご近所さんとバッタリ。踏切りまでおしゃべりして私は駅へ、彼女は教会へ。「辞め時」について話していて中断。 JRは今日も上下線が遅延。それでも時間までに到着し、ほっ。駅までは送迎車。 ウォーミングアップの公園の向いは今年も見事な藤! 最近裏山に猪が4頭出たそうです。クワバラクワバラ 放課後(?) 駅近くの神武寺へ。別のサークルのための下見です。特養せせらぎの前庭に数えきれないほどの大きな鯉のぼりが空を隠していました。
来月以降開催
・長岡智津子さんの投稿
 写真1件
写真1件
・柳澤 光宏さんの投稿
 毎年開催しているシナノ工場祭のご案内(^.^) 5月16日9時からです‼️ 今年はクラフトもの作り体験が全てリニューアル。お子様に喜んでもらえるかと。 アウトレットも色々用意していると聞いています。 お待ちしております(^.^)
毎年開催しているシナノ工場祭のご案内(^.^) 5月16日9時からです‼️ 今年はクラフトもの作り体験が全てリニューアル。お子様に喜んでもらえるかと。 アウトレットも色々用意していると聞いています。 お待ちしております(^.^)
2.PW関連学術ニュース
2-1)生涯にわたる認知能力向上とアルツハイマー病認知症の発症、認知老化、および認知回復力との関連性
***以下は、大阪大学宮坂昌之先生の2026年4月13日のFB投稿です***
認知機能は加齢とともに低下してきますが、積極的に頭を使うことによって認知機能の低下が遅くなるだけではなく、認知機能がむしろ向上し、認知症の発症が遅くなるのではないかと言われています。しかし、それを大規模な調査で科学的に示した例は多くありません。
専門誌Neurologyの近刊に、アメリカ・イリノイ州北東部の高齢者を対象とした認知症に関する経時的臨床病理学的研究の結果が載っています(https://www.neurology.org/doi/10.1212/WNL.0000000000214677)。
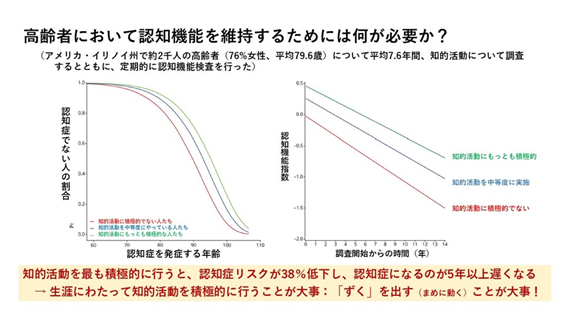
対象者は、調査開始時点で認知症がなく、その後生涯にわたって認知機能向上活動に関するアンケートに回答し、さらに毎年、認知症に関する臨床評価を受けていた人たち約2千人(女性76%、平均年齢79.6歳)です。高齢になってから行った知的活動が非常に多かった人、中等度だった人、低かった人に分けて認知症の発症頻度、発症年齢など3群に分けて、一人平均7.6年にわたり調査しました。
その結果、若い時から知的活動において積極的であっただけでなくて高齢になってからも知的活動を最も積極的に続けた人たちでは、知的活動が少なかった人たちよりも、認知症になるのが38%減り、軽度認知障害も36%低下し、認知障害の発症が5-8年遅くなっていました。つまり、生涯にわたって知的活動を積極的に続けることが認知機能低下の速度を遅くさせ、認知症リスクを低下させることにつながっていた、という結果です。
ということは、年を取ったからもういろいろなことは諦めるというのではなくて、スマホも結構、パソコンも結構、唄を歌うのも結構、習字をするのも結構、手紙を書くのも結構、社会的活動をするのも結構、そのようなことの積み重ねが、加齢による認知機能の低下を遅らせ、ひいてはアルツハイマー型認知症のリスクを下げてくれることにつながる、ということです。年寄りに大事な「きょうよう(今日用事があること)」や「きょういく(今日行くところがあること)」は、いずれも認知機能を高める活動そのものです。長野県の方言で「ずくを出す」という表現がありますが、「まめに動く」という意味です。皆さん、ずくを出して活動しましょう!
関連情報:原論文
掲載誌:Neurology
公開日:March 10, 2026
表題:Associations of Lifetime Cognitive Enrichment With Incident Alzheimer Disease Dementia, Cognitive Aging, and Cognitive Resilience
(和訳:生涯にわたる認知能力向上とアルツハイマー病認知症の発症、認知老化、および認知回復力との関連性)
著者:Andrea R. Zammit , Lei Yu , Victoria N. Poole, Alifiya Kapasi , Robert S. Wilson , and David A. Bennett
https://doi.org/10.1212/WNL.0000000000214677
要旨
背景と目的
生涯にわたる認知的刺激が、その後の人生における認知機能に及ぼす影響は、包括的に調査されていません。本研究の目的は、生涯にわたる認知的刺激とアルツハイマー病(AD)認知症および認知機能低下との関連性を検証すること、そして剖検を受けた死亡者のサブセットにおいて、生涯にわたる刺激とADおよび関連認知症(ADRD)の病理学的指標、ならびに認知回復力(一般的なADRD病理を調整した後の低下)との関連性を探ることでした。
方法
これは、イリノイ州北東部の高齢者を対象とした縦断的な臨床病理学的研究であり、ラッシュ記憶・加齢プロジェクトに参加し、ベースライン時点で認知症がなく、生涯にわたる生活の質の向上を反映したアンケートに回答し、毎年臨床評価を受けていた。我々は、生涯にわたる認知機能の向上を反映した複合指標を作成し、比例ハザードモデルを用いて新規発症AD認知症との関連性、加速故障時間モデルを用いてAD認知症発症の平均年齢との関連性、線形混合効果モデルを用いて認知機能低下との関連性を検証した。死亡した被験者群では、生涯にわたる認知機能の向上と9つのADRD病理および認知回復力との関連性を検証した。
結果
参加者(n = 1,939、女性 75%、ベースライン時の平均年齢 = 79.6)は平均 7.6 年間の追跡調査を完了し、その間に 551 人の参加者が AD 型認知症を発症しました。生涯の充実度が 1 単位高いと、AD 型認知症を発症するリスクが 38% 低下しました (ハザード比 0.62、95% CI 0.52–0.73、p < 0.001)。生涯の充実度が高い (90 パーセンタイル) 場合、低い (10 パーセンタイル) 場合と比較して、AD 型認知症の発症が平均 5 年遅れました。生涯の充実度は、ベースライン時の認知機能 (推定値 = 0.31、SE = 0.02、p < 0.001) および認知機能低下の速度が遅いこと (推定値 = 0.02、SE = 0.01、p = 0.002) と正の相関がありました。死亡者群(n = 948)では、生涯にわたる認知能力向上は神経病理学的指標との有意な関連を示さなかったが、死亡直前の認知機能の高さ(推定値 = 0.32、SE = 0.06、p < 0.001)および病理を調整した後の認知機能低下の速度の遅さ(推定値 = 0.014、SE = 0.01、p = 0.02)と関連していた。
議論
生涯にわたる認知能力向上への取り組みは、アルツハイマー病(AD)認知症のリスク低下および認知機能低下速度の遅延と関連しており、一般的なADRD病理を調整した後でも、生涯にわたる認知能力向上によって高い回復力がもたらされることが示唆された。本研究の結果は、晩年の認知機能の健康は、生涯にわたる認知能力向上への取り組みによって部分的に左右されることを示唆している。
2-2)岐阜大学医学部下畑先生からの最新医学(2026年4月)
・ナノプラスチックの脳への侵入とミクログリアによる防御,そして認知症につながる?
****岐阜大学医学部下畑先生の2026年4月1日のFB投稿より****
 ナノプラスチックが脳に与える影響を,侵入と防御の両面から理解できる2つの論文を紹介します.いずれも本邦からで,一つは国立環境研究所のItoらによる研究で,もう一つは国立精神・神経医療研究センターおよび東京大学を中心としたOgakiらの研究です.
ナノプラスチックが脳に与える影響を,侵入と防御の両面から理解できる2つの論文を紹介します.いずれも本邦からで,一つは国立環境研究所のItoらによる研究で,もう一つは国立精神・神経医療研究センターおよび東京大学を中心としたOgakiらの研究です.
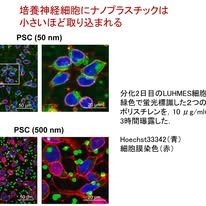
まずItoらの研究は,「ナノプラスチックは神経細胞に入るのか?」という問いに答えたものです.結論としては,ヒト由来神経細胞(LUHMES)を用いた実験により,ポリスチレンナノ粒子は神経細胞内に取り込まれることが明確に示されました.特に50 nmの粒子は500 nmに比べて圧倒的に効率よく取り込まれ,取り込み量は数百倍に達しました(図1).取り込みは主にクラスリン依存性エンドサイトーシスやマクロピノサイトーシスによるものでした.さらに,取り込まれた粒子は主にリソソームに局在し,一部はミトコンドリア周囲にも分布していました.また細胞種による違いが認められ,ミクログリアが最も高い取り込み能を示し,神経幹細胞がこれに続き,分化した神経細胞やアストロサイトでは取り込みが比較的低いという結果でした.特に神経幹細胞で取り込みが高いという所見は,発達期における脆弱性を示唆するものとして重要です.
一方で,これほど細胞内に取り込まれるにもかかわらず,急性毒性はほとんど認められず,細胞生存率,神経突起伸長,酸化ストレスへの明確な影響は確認されませんでした.しかしこれは安全ということではありません.神経細胞がナノプラスチックを取り込み,リソソームに蓄積するという事実は,神経細胞自身ではこれを十分に処理できず,ミクログリアなどのクリアランス機構に依存していることを示唆しています.このバランスが破綻した場合,長期的な蓄積や神経変性疾患との関連が生じる可能性があり,重要な知見と考えられます.
つぎにOgakiらの研究は,ナノプラスチックを含むナノ粒子が脳に侵入した後に「脳がどのように対処しているか」を明らかにしたものです.ナノ粒子は血流を介して脳内に到達し,特に視床や視床下部に蓄積することを示しました(図2).そしてこに蓄積に対してミクログリアが貪食を行いますが,その際に重要なのが補体C3による「タグ付け」です.ナノ粒子にC3が付着すると,ミクログリアは補体受容体CR3を介してそれを選択的に取り込みます.さらにこのC3は,血管内皮細胞から分泌されるCCL17がアストロサイトのCCR4を活性化することで産生されることが示されました.つまり,「血管内皮→アストロサイト→補体→ミクログリア」という連携機構が存在し,ナノ粒子の除去に働いていることが明らかになりました(図3).この機構の意義を最も明確に示しているのが図3で,CCR4を選択的アンタゴニストC-021で阻害するとミクログリアによるナノ粒子の除去が低下した結果,神経細胞死の増加と不安様行動の増悪が生じることが示されています(図4).すなわち,この機構は単なる異物処理ではなく,神経保護として機能している点が重要です.
ここで近年報告され注目を集めた「認知症患者の脳でナノプラスチックが多量に蓄積している(Nat Med. 2025;31:1114-1119.)」という観察結果を踏まえると,これら2つの研究は非常に重要な意味を持ちます.Itoらの研究は,ナノプラスチックが実際に神経細胞内に取り込まれ得ることを示しており,一方でOgakiらの研究は,それを除去する脳の防御機構が存在することを示しています.すなわち,ナノプラスチックの脳内蓄積は,「侵入」と「除去」のバランスで決まると考えることができます.この観点から認知症を考えてみると,アルツハイマー病をはじめとする神経変性疾患では,ミクログリア機能の低下や補体系の異常,さらには血管障害や血液脳関門の破綻が知られています.このような状態では,ナノ粒子に対するC3によるタグ付けやミクログリアによる貪食が十分に機能せず,クリアランスが低下する可能性があります.その結果として,ナノプラスチックが脳内に蓄積しやすくなると考えることができます.そしてナノプラスチックが神経炎症や細胞機能障害を引き起こすことで,アミロイドβやタウ病理を促進し,神経変性を悪化させる可能性もあります.つまりナノプラスチックの蓄積は,認知症において結果でもあり,原因でもありうると考えられます.
以上より,ナノプラスチックの脳への影響は,「神経細胞への侵入」,「ミクログリアを中心としたクリアランス機構」,そして「その破綻としての神経障害」という3つの視点から理解する必要があります.すなわち,ナノプラスチックは単に毒性を持つか否かではなく,「脳がそれをどこまで処理できるか」という動的な均衡の中で影響を及ぼしている可能性があります.よって本テーマは環境問題にとどまらず,神経変性疾患の新たな修飾因子としての可能性を含んでいます.
Ogaki A, Kinoshita S, Ikegaya Y, Koyama R. Chemokine-complement cascade in glial-vascular units protects neurons from non-biogenic nanoparticles. J Neuroinflammation. 2025;22(1):182. PMID: 40660294.
Ito T, Ikuno Y, Udagawa O, Tanaka K, Kurokawa Y, Kakeyama M, Maekawa F. Human neurons are susceptible to the internalization of small-sized nanoplastics. Environ Toxicol Pharmacol. 2025;118:104776. PMID: 40744315.
Nihart AJ, Garcia MA, El Hayek E, et al. Bioaccumulation of microplastics in decedent human brains. Nat Med. 2025 Apr;31(4):1114-1119. PMID: 39901044.
・健康ONEクリップ しびれの原因がわかる「しびれ図鑑」 今晩放送です!
****岐阜大学医学部下畑先生の2026年4月1日のFB投稿より****
 NHKのトリセツショー「あなたの「しびれ」はどれ?解消&予防SP」にて「しびれ図鑑」を作成しましたが,この番組とは別枠で,図鑑の内容を一部抜粋した3分VTRが放送されることになりました.今後,番組と番組の間などで随時流れることになるそうです.まず1回目の放送が本日の夜になります.もしよろしければご覧ください.この「しびれ図鑑」はとても好評で,今回の企画になったようです.ぜひ「しびれ図鑑」をご活用ください.
NHKのトリセツショー「あなたの「しびれ」はどれ?解消&予防SP」にて「しびれ図鑑」を作成しましたが,この番組とは別枠で,図鑑の内容を一部抜粋した3分VTRが放送されることになりました.今後,番組と番組の間などで随時流れることになるそうです.まず1回目の放送が本日の夜になります.もしよろしければご覧ください.この「しびれ図鑑」はとても好評で,今回の企画になったようです.ぜひ「しびれ図鑑」をご活用ください.
放送日:4月1日(水)午後10:57~
★リンクはコメント欄をご覧ください.
#NHK #トリセツ #しびれ図鑑
・せん妄は「脳の老廃物排出機能の障害」だったのか!?―グリンファティック仮説が示す新しい理解
****岐阜大学医学部下畑先生の2026年4月3日のFB投稿より****
 Nat Rev Neurol誌のPerspectiveに面白い仮説提唱論文が出ています.3人の先生の共著ですが,最後がグリンファティック系の提唱者として知られるMaiken Nedergaard先生であり,注目して読みました.せん妄の病態を「グリンファティック機能障害」という観点から統一的に説明しようとする,非常に意欲的な論文でした.
Nat Rev Neurol誌のPerspectiveに面白い仮説提唱論文が出ています.3人の先生の共著ですが,最後がグリンファティック系の提唱者として知られるMaiken Nedergaard先生であり,注目して読みました.せん妄の病態を「グリンファティック機能障害」という観点から統一的に説明しようとする,非常に意欲的な論文でした.
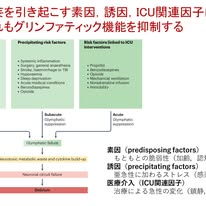
まずせん妄については,入院患者においてしばしば認められる症候で,特にICUでは30~70%と高頻度に認められます.従来,炎症,神経伝達物質異常,睡眠障害などさまざまな機序が提唱されてきましたが,いずれも部分的な説明にとどまり,統一的な理解には至っていませんでした.この論文ではこれらを一つの枠組みで捉え直し,せん妄を急性の「脳の老廃物排出機能の障害」として理解することを提案しています.
その鍵となるのがグリンファティック系です.これは脳内の血管周囲腔を介して脳脊髄液が流入し,間質液と混合したのちに静脈周囲やリンパ系へ排出されることで,アミロイドβやタウ,炎症性サイトカインなどの神経毒性物質を除去するシステムです.この機構はアストロサイトのAQP4水チャネルに依存し,さらに心拍や呼吸に伴う脳の拍動によって駆動されます.特に重要なのは,このシステムが睡眠中に最も活発に働き,覚醒時には抑制されるという点です.
この論文の仮説は,せん妄とはこのグリンファティック機能が急性に低下した状態であり,その結果として脳内に神経毒性物質や炎症性サイトカインが蓄積し,神経ネットワークの同期やシナプス機能が障害されることで発症するというものです.この考え方の優れている点は,既知の危険因子がすべてこの機構に収束されることを示した点にあります.すなわち,加齢や認知症,心血管疾患,腎不全といった「素因」は慢性的にグリンファティック機能を低下させており,そこに感染や手術,外傷といった急性の「誘因」が加わることで,機能はさらに抑制されます.
加えて,「ICUで行われる医療介入」そのものが,この機能を強く抑制する可能性があります.鎮静薬やオピオイドは睡眠構造を乱し,ノルアドレナリンは覚醒状態を維持することでグリンファティック系を抑制します.また人工呼吸の陽圧換気では胸腔内圧が上昇し,静脈血が頭蓋内にうっ滞しやすくなるため,頭蓋内圧が上がり,血管周囲腔が圧迫されます.その結果,脳脊髄液の流れが悪くなります.ICUではこれらが同時に存在するため,結果として脳の「排出機能」は多重に抑制されることになります.
この病態を最も明確に示しているのが下図です.この図では,まず加齢や基礎疾患によってもともとグリンファティック機能が低下している状態(素因)があり,そこに感染や外傷などの急性ストレス(誘因)が加わり,さらにICUでの鎮静や人工呼吸,睡眠障害といった医療介入(ICU関連因子)が重なることで,グリンファティック機能が,それぞれ,元来(初めから)/亜急性に/急性に低下することになります.その結果,脳内に老廃物や炎症性サイトカインが蓄積し,神経回路の機能が破綻してせん妄が発症するという流れです.
せん妄が夜間に目立つことも,この仮説から説明できます.本来,睡眠中には細胞外間隙が拡大し,脳脊髄液の流入が増加することで老廃物の除去が促進されます.しかしICUでは睡眠が著しく断片化し,徐波睡眠やREM睡眠が減少しており,本来夜間に働くべきグリンファティック機能が十分に発揮されません.さらに覚醒状態ではノルアドレナリンが高く,この機能は抑制されます.その結果,「本来なら脳が回復するはずの夜に回復できない」状態が生じ,老廃物の蓄積が進み,せん妄症状が顕在化しやすくなると考えられます.
また,せん妄と神経変性疾患との関連にも言及しています.グリンファティック機能の低下はアルツハイマー病やパーキンソン病,ALSなどでも認められており,老廃物の蓄積と密接に関係しています.せん妄はこうした脆弱な脳において発症し,その後の認知機能低下や認知症リスクを高めることが知られていますが,その背景にはグリンファティック機能のさらなる障害が関与している可能性があります.すなわち,せん妄のエピソード自体が神経変性の進行を加速させる可能性が示唆されています.
治療的な観点から考えると,鎮静を最小限にし,可能な限り覚醒状態を保つこと,睡眠を維持すること,早期離床を促すことなどは,いずれもグリンファティック機能を維持する方向に働き有効と考えられます.薬剤としてはデクスメデトミジンが注目されます.この薬剤はα2アドレナリン受容体作動薬であり,青斑核の活動を抑制することでノルアドレナリンを低下させ,自然睡眠に近い鎮静状態をもたらします.その結果,グリンファティック機能を比較的保ちやすい可能性があり,実際にせん妄の発症を減少させることが報告されています.逆にプロポフォールやベンゾジアゼピンは深い鎮静をもたらすものの,睡眠とは異なる状態であり,グリンファティック機能を抑制する可能性があります.
もしかしたらせん妄は「避けられない合併症」ではなく,「脳の環境を整えることで予防・軽減できる可能性のある病態」として再定義されるかもしれません.今後そのような視点で,せん妄の予防・治療を行ってみたいと思います.
Boesen HC, Du T, Goldman SA, Nedergaard M. Glymphatic dysfunction: a unifying hypothesis for delirium. Nat Rev Neurol. 2026 Mar 30. PMID: 41912735.
・ラモトリギンとレベチラセタムの用量は妊娠中・産後にどう変えるべきか? MONEAD研究より
****岐阜大学医学部下畑先生の2026年4月4日のFB投稿より****
 妊娠中のてんかん診療では,「どのタイミングでどの程度薬剤を増減すべきか」という問いに直面します.妊娠中は腎血流や肝代謝の変化,蛋白結合の低下,グルクロン酸抱合の亢進などにより,多くの抗てんかん薬(ASM)でクリアランスが増加します.このため,同じ用量でも血中濃度が低下し,発作増悪のリスクが生じます.一方で,分娩後はこれらの変化が急速に元に戻るため,増量したままでは過量投与となる危険があります.今回紹介するNeurology誌の論文は,ASMの適切な調整という問いに対して重要な示唆を与える研究です.米国のUniversity of Pittsburghなど20施設からなるMONEAD研究グループによって実施されました.
妊娠中のてんかん診療では,「どのタイミングでどの程度薬剤を増減すべきか」という問いに直面します.妊娠中は腎血流や肝代謝の変化,蛋白結合の低下,グルクロン酸抱合の亢進などにより,多くの抗てんかん薬(ASM)でクリアランスが増加します.このため,同じ用量でも血中濃度が低下し,発作増悪のリスクが生じます.一方で,分娩後はこれらの変化が急速に元に戻るため,増量したままでは過量投与となる危険があります.今回紹介するNeurology誌の論文は,ASMの適切な調整という問いに対して重要な示唆を与える研究です.米国のUniversity of Pittsburghなど20施設からなるMONEAD研究グループによって実施されました.
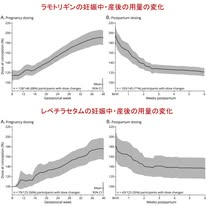
てんかんを合併した妊婦299例を対象とした前向き観察研究で,妊娠中から産後6週までのASMの用量変化を詳細に追跡しています.その結果,妊娠中には全体の約68%で増量が行われ,初回の調整は登録後中央値32日で実施されていました.さらに産後6週以内には約48%で減量が行われ,その開始は中央値3日と非常に早期でした.この「妊娠中は増量し,産後は速やかに減量する」というダイナミックな用量変化が,本研究の重要なメッセージです.
催奇形性の少なさから,特にラモトリギンとレベチラセタムが本研究の中心的評価薬剤となっています.ラモトリギンでは87.7%の症例で増量が行われ,1回あたり中央値100 mg/日の増量を繰り返しながら,分娩時には妊娠前の約191%に達していました.図1にはこの変化が明瞭に示されており,妊娠週数の進行とともに用量が連続的に上昇していく様子が理解できます.縦軸の“dose at conception”は妊娠成立時点の用量を基準とし,その後の用量変化を割合(%)で表したものです.例えば妊娠成立時に200 mg/日であった場合,分娩時に400 mg/日であれば200%となります.さらに重要なのは産後の用量変化であり,分娩直後から急速に減量が行われています.ただし6週時点でも約116%と,完全には妊娠前の用量に戻っていない点は臨床的に重要です.
レベチラセタムでも同様の傾向が認められますが,いくつかの相違もみられます.56%で増量が行われ,1回あたり中央値500 mg/日の増量により,分娩時には妊娠前の177%に達しています(図2).一方,産後の減量はラモトリギンほど急峻ではなく,6週時点でも136%と比較的高い水準に維持されています.これはレベチラセタムでは高用量でも副作用が出現しにくいことが影響している可能性が指摘されています.
このような積極的な用量調整のもとで,妊娠中の発作増悪の頻度は非妊娠時と同程度に保たれており,発作コントロールの維持に有効であったと考えられます.さらに児の神経発達も良好であり,特にラモトリギンおよびレベチラセタムの単剤治療例では,6歳時の言語発達指標に有意差は認められませんでした.
本研究から得られる臨床的示唆は明確です.すなわち,妊娠中は4〜6週間隔での用量調整を前提に,必要に応じて適切に増量すること,そして産後は数日以内に減量を開始することが重要であるということです.さらに,産後も直ちに妊娠前の用量に戻すのではなく,睡眠不足などの発作誘発因子を考慮しつつ,やや高めに維持するという判断も示唆されます.
ただし,本研究は観察研究であり,用量調整の判断基準(血中濃度か臨床症状か)が明確ではないことなどの限界もあります.しかしそれでも,専門施設における実際のASM調整の実態を具体的に示した点で,非常に貴重な研究といえます.特に図1および図2は,本研究のエッセンスを直感的に理解できる優れた図であり,ぜひご確認いただきたいと思います.
Pennell PB, Li D, Kerr WT, et al. Antiseizure Medication Dosing Strategy During Pregnancy and Early Postpartum in Women With Epilepsy in MONEAD. Neurology. 2026 Jan 27;106(2):e214483. PMID: 41461064.
・腰痛:「見逃してはならない病態」と画像検査前の診察のコツ
****岐阜大学医学部下畑先生の2026年4月7日のFB投稿より****
 腰痛の多くは自然軽快する筋骨格性疼痛ですが,一部には神経障害や重篤な疾患が隠れています.今週号のNEJM誌に掲載された整形外科のエキスパートによる動画・論文は,腰椎診察の実践的なコツを示した有用な内容で勉強になりました.とくに「見逃してはならない病態」と,画像検査前の診察のコツを体系的に整理しています.
腰痛の多くは自然軽快する筋骨格性疼痛ですが,一部には神経障害や重篤な疾患が隠れています.今週号のNEJM誌に掲載された整形外科のエキスパートによる動画・論文は,腰椎診察の実践的なコツを示した有用な内容で勉強になりました.とくに「見逃してはならない病態」と,画像検査前の診察のコツを体系的に整理しています.
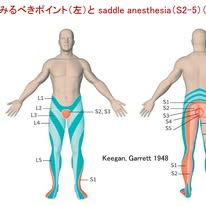
まず最も重要なのは,「見逃してはならない病態」を見抜くことです.病歴で特に重視すべきはred flagのチェックです.具体的には,馬尾症候群を示唆する排尿・排便障害,saddle anesthesia,下肢筋力低下,さらに感染や腫瘍を示唆する発熱,体重減少,癌の既往の6つを挙げています.なかでも排尿障害やsaddle anesthesiaは馬尾症候群を強く示唆する所見であり,緊急対応が必要です.saddle anesthesiaとは,肛門や会陰,内股にかけて,ちょうど馬の鞍が接触する領域に一致した感覚障害であり,仙髄(S2〜S5)の障害を反映します.患者はこの部位の異常を自ら訴えないことも多く,「陰部や肛門周囲の感覚に違和感はありませんか?」と積極的に確認することが重要です.また発熱や体重減少,癌の既往があれば,感染や腫瘍といった全身性疾患を常に念頭に置く必要があります.
診察は視診から始まります.患者を立位にして後方から観察すると,肩と骨盤の高さの左右差や脊柱の傾きが評価できます.そして重要なのが姿勢です.腰椎前弯が失われると体幹は前方へ傾きますが,それを補うために骨盤は後傾(pelvic retroversion)し,股関節や膝関節は屈曲し,足関節は背屈するという一連の代償機構が働きます.図1左ではこの「姿勢保持のための代償機構」が示されており,腰痛患者にみられる前かがみ姿勢が,単なる痛み回避ではなく,全身のバランスを保つための適応であることが理解できます.つまり姿勢そのものが診断の手がかりになります.例えば,前かがみであれば脊柱管狭窄,体を横に傾けていれば神経根障害,膝を曲げて立っていれば脊柱アライメントの破綻が推測されます.
つぎは歩行です.Trendelenburg歩行は,股関節外転筋の機能低下により骨盤を安定して支えられず,体を左右に傾けながら歩く状態であり,L5神経根障害や股関節疾患を示唆します.また歩行障害が顕著な場合には,腰椎病変だけでなく頸髄症など中枢病変の可能性も考慮する必要があります.
触診では棘突起の圧痛と傍脊柱筋の圧痛を区別します.前者は骨折や腫瘍,後者は筋・筋膜性疼痛を示唆し,原因の絞り込みに有用です.可動域では前屈,後屈,側屈,回旋を評価し,疼痛や左右差を確認します.
神経診察ではデルマトームとミオトームの評価が中心となります.図1右は教科書的なデルマトームで,L4は下腿内側,L5は足背,S1は足底外側に対応し,「どこがしびれるか」から障害神経根を推定することができます.筋力ではL2の股関節屈曲からS1の足関節底屈まで順に評価し,腱反射では膝蓋腱反射(L4)とアキレス腱反射(S1)を確認します.反射低下は神経根障害を示唆し,反射亢進があればより上位の中枢病変の可能性を考慮します.
誘発試験としてはstraight leg raising test(SLR test)が重要で,坐骨神経の伸張によりL5やS1神経根障害を検出します(図2左A).足関節を背屈させることで神経の伸張はさらに増強され(図2左B),逆に膝を曲げると伸張は緩和されますが,膝窩部に圧を加えると再び症状が誘発されます(図2左C・D).SLR testは仰臥位で行うのが基本ですが,動画(写真)のように座位でも同様に評価が可能であり,両者を組み合わせることで診断精度を高めることができます.仰臥位では陽性であるにもかかわらず座位では陰性となる場合は,神経の伸張という観点からは説明がつきにくく,非器質的要因の関与,いわゆる「Waddell徴候」を示唆する重要な所見です.さらに,femoral nerve stretch testは大腿神経を伸張することでL3やL4神経根障害の評価に有用であり(図2右A・B),SLR testとあわせて上下の腰椎レベルを見分けるうえで重要な手技です.
腰痛診療においては,まず患者を観察し,しびれの分布と姿勢の意味を読み取ることが重要です.デルマトームは神経の局在を示し,姿勢は力学的破綻を示します.そして誘発試験はそれを確かめる手段です.患者の立ち方や動き方を丁寧に観察すれば,画像検査を行う前から,診断の手がかりはすでに示されているといえます.
Daniels AH, et al. Clinical Examination of the Lumbar Spine. N Engl J Med. 2026 Apr 2;394(13):e23. PMID: 41931050.
・「除去」から「排出」へ:グリンファティック系を再起動するアルツハイマー病新治療がヒトで実現する!?
****岐阜大学医学部下畑先生の2026年4月8日のFB投稿より****
 アルツハイマー病(AD)の病態を「異常タンパク質の蓄積」という静的な視点から,「排出システムの破綻」という動的な視点へと大きく転換させる画期的な臨床研究(プレプリント)が報告されました.Applied Cognition社,スタンフォード大学やワシントン州立大学など,脳神経内科,睡眠医学,生理学の専門家が集結した学際的チームによって実施された研究です.これまでAD治療の関心の中心は蓄積したアミロイドβ(Aβ)を直接除去する抗体療法でしたが,この研究は脳の天然の掃除システムである「グリンファティック系」を薬剤で強化し,老廃物を「そもそも蓄積させない」あるいは「効率よく排出させる」という画期的で,より生理的なアプローチを提示しています.
アルツハイマー病(AD)の病態を「異常タンパク質の蓄積」という静的な視点から,「排出システムの破綻」という動的な視点へと大きく転換させる画期的な臨床研究(プレプリント)が報告されました.Applied Cognition社,スタンフォード大学やワシントン州立大学など,脳神経内科,睡眠医学,生理学の専門家が集結した学際的チームによって実施された研究です.これまでAD治療の関心の中心は蓄積したアミロイドβ(Aβ)を直接除去する抗体療法でしたが,この研究は脳の天然の掃除システムである「グリンファティック系」を薬剤で強化し,老廃物を「そもそも蓄積させない」あるいは「効率よく排出させる」という画期的で,より生理的なアプローチを提示しています.
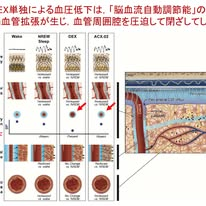
研究チームは,55〜64歳の健常高齢者を対象とした厳密なクロスオーバー試験を実施しました .ここで検証されたのは,α2受容体刺激作用を持つ鎮静剤のデクスメデトミジン(DEX;プレセデックス®)と,末梢血管を収縮させて血圧低下を防ぐミドドリンを組み合わせた複合薬「ACX-02」の効果です.DEHは標準的な臨床用量(0.7 micro-g/kg/h)です.DEXは脳内のノルアドレナリンを抑制することで,老廃物を押し出す動力源となる睡眠徐波を劇的に増加させることや,脳組織の細胞外スペースを拡大させることが動物実験で示されており,これがヒトでは「脳実質抵抗」を低下させる(通り道を広げる)効果として期待されていました.またミドドリンが必要な理由は後述しますが,DEXによる「逆効果となる脳血管の拡張」を防ぎ,老廃物の通り道を確保するためです.
被験者はあえて一度睡眠不足の状態に置かれた後,日中に短時間の睡眠機会を与えられ,その間の生理計測と血液バイオマーカーの精密な測定が行われました.つまり「脳の掃除スイッチが最大に入る状態」を人為的に作り出し,薬剤の効果を正確に追跡したわけです.薬剤の効果は脳波(睡眠徐波,相対パワー)と,流体力学的な指標(脳実質抵抗,脳血管コンプライアンス),血液バイオマーカー(Aβ42/Aβ40比,p-tau217)で検討しています.
さて結果ですが,DEXを単独で投与した場合,睡眠中の徐波活動は有意に増加したものの,脳からのAβやタウの排出増加は認められませんでした.この現象の鍵を握るのが,図1の生物学的メカニズムです.DEX単独投与による血圧低下した際に,全身の血圧が変動しても脳への血流を一定に保とうとする「脳血流自動調節能」があるため,代償的反応として脳血管は抵抗を下げて血流を維持する方向に働きます.つまり血管拡張が生じますが,それが老廃物の通路である血管周囲腔を物理的に圧迫して閉ざしてしまう様子が描かれています.つまり,単に深い眠りを誘発するだけでは不十分であり,血管動態を含めた統合的な制御が不可欠であることが明らかになったわけです.
これに対し,ACX-02を用いた介入では,ミドドリンの作用によって血圧低下が抑制され,脳血管の過剰な拡張が回避されました.その結果,図2に示されるデータが証明するように,劇的な変化が生じました.つまり図2Aで徐波カウントが顕著に増加する一方で,図2Bでは脳内の水の通りやすさの指標である「脳実質抵抗(Rp)」がプラセボ比で51.4%も大幅に減少しました.このとき平均動脈圧(MAP)は安定して維持されていました.
最も特筆すべき結果は,この生理的変化が異常タンパクの排出量に直結した点です.ACX-02投与により,Aβ42/Aβ40比およびリン酸化タウ(%p-tau217)で評価したクリアランスが約8〜10%有意に上昇しました.これらの指標は脳から血中への排出動態をダイレクトに反映するものであり,ヒトにおいて短時間の介入で老廃物の除去を定量的に増加させられることを世界で初めて実証しました.ベイズ媒介解析によれば,この効果の最大の要因は脳実質抵抗の低下であり,次いで徐波活動の増加が重要な役割を担っていることが示されています.
この発見は,将来的に大きな臨床意義を持ちます.著者らは,約10%の排出増加が長期的に持続すれば,アミロイド蓄積の進行を数年単位で遅らせ,病理学的閾値に達する時期を大幅に延期できる可能性があると考察しています.また,このアプローチは既存の抗体療法と競合するものではなく,抗体によって可溶化されたタンパク質を,グリンファティック系を介して効率よく排出させるという補完的治療になり得るものです.本研究は,ADを「流れが滞ることで溜まる」疾患と捉え直し,その流れを再び動かすことができるという希望を提示した画期的な研究と言えると思います.
Dagum P, et al. Pharmacological enhancement of glymphatic function in humans increases the clearance of Alzheimer’s disease-related proteins. medRxiv. 2026 Mar 12. doi: 10.64898/2026.03.10.26348048.
・環境神経学の時代;神経変性疾患は「加齢」や「遺伝」だけで説明されるものではなく,「環境との相互作用」の中で発症し進行する疾患である
****岐阜大学医学部下畑先生の2026年4月10日のFB投稿より****
 近年,「パーキンソン・パンデミック」という言葉が注目されています.世界のパーキンソン病(PD)患者数は過去数十年で大きく増加しており,その背景として大気汚染をはじめとする環境要因の関与が注目されています.従来,神経変性疾患は遺伝要因の研究が主体でしたが,現在では「環境との相互作用」という視点が急速に重要性を増しています.今回紹介する3つの研究は,このパラダイムシフトを決定づける重要なものです.
近年,「パーキンソン・パンデミック」という言葉が注目されています.世界のパーキンソン病(PD)患者数は過去数十年で大きく増加しており,その背景として大気汚染をはじめとする環境要因の関与が注目されています.従来,神経変性疾患は遺伝要因の研究が主体でしたが,現在では「環境との相互作用」という視点が急速に重要性を増しています.今回紹介する3つの研究は,このパラダイムシフトを決定づける重要なものです.
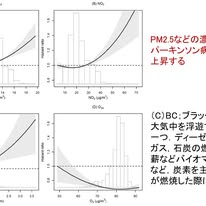
まず,PDに関するデンマークの全国コホート研究(文献1)は,「大気汚染」の影響を人口レベルで示した点で画期的です.約328万人を平均15.7年間追跡し,36,665例の発症を解析した結果,PM2.5,NO₂,ブラックカーボンのいずれにおいても,曝露量の増加と発症リスクとの有意な関連が認められました.特に重要なのは,濃度が高くなるほど発症リスクが上昇する「濃度反応関係」が明瞭に示された点です.図1では,PM2.5濃度の上昇に伴いハザード比が連続的に増加しており,大気汚染が「量」に依存して神経変性リスクを規定する可能性が示唆されています.グラフ下部のヒストグラムを重ねて見ることで,多くの人が実際に曝露されている濃度帯が可視化されています.この点は重要であり,大気汚染による健康被害は高濃度の曝露を受ける一部の集団のみの問題ではなく,より広い集団に影響しうることを示しています.ちなみに4つ目のO₃(オゾン)では負の相関がみられますが,オゾンによる保護作用を示すものではなく,交通由来汚染物質との逆相関や汚染物質間の複雑な相関構造を反映した見かけ上の所見のようです.
では,なぜ大気汚染が脳を蝕むのでしょうか.この問いに対して,JCI誌のPalushajらは,「exposome(エクスポソーム;環境曝露の累積)」という概念を用いて説明しています(文献2).exposomeはexposure(暴露,曝露)と-ome(全体,網羅的な総体) を組み合わせた混成語です.彼らの主張の核心は,「病態の起点は脳ではなく腸にある」という点です(図2).大気汚染粒子や農薬,マイクロ・ナノプラスチックといった環境因子は,腸内環境を攪乱し,腸管バリアを破綻させます.その結果,炎症や免疫異常が誘導され,αシヌクレインの異常凝集が生じ,それが迷走神経を介して中枢神経系へと波及する可能性が示唆されています.実際,PDでは便秘や嗅覚障害といった症状が発症の10〜20年前から出現することが知られており,「腸―免疫―脳軸」を介した病態形成を強く支持しています.
大気汚染の影響はPDにとどまりません.スウェーデンのKarolinska InstitutetによるALSの研究(文献3)は,環境因子が神経変性疾患の「発症」だけでなく「進行」にも関与する可能性を示しました.1,463例のALS患者を対象とした解析では,PM2.5やPM10,NO₂への長期曝露がALS発症リスクの上昇と関連していました.さらに,曝露量が高いほどALSFRS-Rで評価した進行速度が速く,呼吸機能の悪化や死亡リスクの上昇とも関連していました.図3に示すフォレストプロットは,曝露期間ごとに一貫して発症リスクが上昇する様子を示しており,大気汚染がALSの自然歴そのものに影響を与えている可能性を強く示唆しています.
以上を統合すると,一つの明確なメッセージが浮かび上がります.神経変性疾患は,もはや「遺伝」や「加齢」だけで説明される疾患ではなく,「環境との相互作用」の中で発症し進行する疾患であるということです.今後の神経内科学においては,患者の遺伝的背景だけでなく,「どのような環境に曝露されてきたか」を問う視点が必要になります.疾患予防を目指すのであれば,大気汚染,農薬,重金属,さらには話題のマイクロ・ナノプラスチックといった「見えないリスク」に対し,個人レベルの予防に加え,社会全体での対策が求められるということです.つまり神経変性疾患の理解は,「環境神経学(environmental neurology)」という新しい枠組みへと大きく舵を切りつつあるのだと思います.我が国における神経変性疾患の「パンデミック」を防ぐためにも,この潮流を認識する必要があります.
1. Cole-Hunter T, et al. Long-Term Exposure to Air Pollution and Incidence of Parkinson’s Disease. Movement Disorders. 2026. PMID: 38472866
2. Palushaj B, Voigt RM. The Parkinson’s pandemic: prioritizing environmental policy and biological resilience via the gut. J Clin Invest. 2026;136:e205275
3. Wu J, et al. Long-Term Exposure to Air Pollution and Risk and Prognosis of Motor Neuron Disease. JAMA Neurol. 2026;83:213-222. PMID: 39724566
・一度のCAR-Tで3つの自己免疫疾患が寛解した!:自己免疫疾患はB細胞を一度リセットして長期寛解を目指す時代に入る!?
****岐阜大学医学部下畑先生の2026年4月12日のFB投稿より****
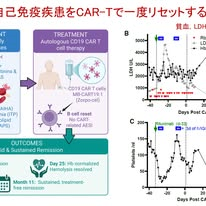 話題になっているドイツからのMed誌に掲載された症例報告です.重症かつ治療抵抗性の自己免疫性溶血性貧血(AIHA)に,免疫性血小板減少症(ITP)と抗リン脂質抗体症候群(APS)を合併した47歳女性に対し,自己由来CD19 CAR-T細胞療法を行い,3つの自己免疫疾患すべて速やかに寛解したという報告です.自己免疫疾患治療の考え方を大きく変える可能性を秘めた,非常に注目すべき報告です.
話題になっているドイツからのMed誌に掲載された症例報告です.重症かつ治療抵抗性の自己免疫性溶血性貧血(AIHA)に,免疫性血小板減少症(ITP)と抗リン脂質抗体症候群(APS)を合併した47歳女性に対し,自己由来CD19 CAR-T細胞療法を行い,3つの自己免疫疾患すべて速やかに寛解したという報告です.自己免疫疾患治療の考え方を大きく変える可能性を秘めた,非常に注目すべき報告です.
この患者さんは,寒冷凝集素型(IgM)と温式(IgG)の両方の自己抗体を伴う重症AIHAに加え,ITPとAPSも合併していました.診断後10年以上にわたり,ステロイド,リツキシマブ,免疫抑制薬など計9種類の治療を受けても改善せず,CAR-T導入前には1日1〜3単位の輸血を要する,まさに生命の危機にある状態でした.
今回用いられたCD19 CAR-T療法は,白血病や悪性リンパ腫で使われているCAR-Tと基本的な技術は同じです.患者さん自身のT細胞を採取し,B細胞表面抗原であるCD19を認識する人工受容体(CAR)を遺伝子導入し,体外で増殖させてから体内に戻します.今回使用された製剤はzorpocabtagene autoleucel(Zorpo-cel),すなわち自家白血球由来の遺伝子改変CAR-T細胞で,投与量は1×10^6/kgでした.
「がんのCAR-T」と「自己免疫疾患のCAR-T」は細胞こそ同じでも,治療の目的が異なります.がんでは,CD19を持つ悪性B細胞そのものを根絶することが目的です.一方,自己免疫疾患では,CD19を持つ異常B細胞が自己抗体を作り続けることで病気が維持されています.つまり,今回のCAR-T療法は,病的な自己抗体を作るB細胞と,その異常な免疫記憶を一度深く取り除き,「免疫系を初期化すること」を目指した治療といえます.リツキシマブ(抗CD20抗体)もB細胞を標的としますが,すべてのB細胞系統を十分に除去できるわけではなく,再燃することも少なくありませんが,CAR-Tはより深いB細胞枯渇と免疫リセットをもたらすことが期待されます.
実際の治療としては,CAR-T投与前に,フルダラビンとシクロホスファミドによるリンパ球除去療法も行われました.これは単なる前処置ではなく,CAR-T細胞を体内でしっかり増殖・定着させるための重要な準備です.もともと体内にいるリンパ球を一時的に減らすことで,CAR-T細胞が入り込む余地を作り,さらにCAR-Tの増殖を助けるサイトカイン環境を整えるそうです.
そして治療効果は驚くほど迅速でした.投与後7日目には輸血が不要となり,長年続いていた輸血依存状態から脱却しました.2週間後には全身状態が速やかに改善しました.25日後にはヘモグロビン値が正常化し,溶血マーカーも改善しました.さらに,寒冷凝集素抗体価は低下し,病的に高値であった抗リン脂質抗体も時間とともに正常化しました.血小板数も追加治療なしで安定し,ITPも改善しました.11か月以上の経過観察で,再燃なく,薬剤を一切使わない完全寛解が維持されています.
図は,今回の治療をまとめたものです.まず治療前の多剤抵抗性のAIHA,ITP,APSにより生命を脅かされていた状態が示され,つぎにCD19 CAR-T細胞による「B細胞リセット」を行い,幸い特に注目すべき有害事象(Adverse Event of Special Interest;AESI)は認めませんでした.そして転帰としては投与7日で輸血不要,25日でヘモグロビン正常化,11か月以上無治療寛解という経過がわかります.懸念されたAESIとしては,サイトカイン放出症候群(CRS)や免疫エフェクター細胞関連神経毒性症候群(ICANS)が挙げられますが,本例ではいずれも認めませんでした.一因として,自己免疫疾患では,がんと比較して標的細胞量が少ない可能性が考えられます.
今回の症例は,「自己免疫疾患は免疫抑制剤により一生抑え続けるもの」という今までの考え方に対し,「一度リセットして長期寛解を目指す」という新しい発想を提示しました.もちろんまだ1例報告ですし,病気によっては自己抗体を認めてもT細胞や自然免疫が主役の疾患もあり,すべての自己免疫疾患に使えるのか分かりません.長期安全性,感染症リスク,費用対効果など多くの課題も残されていますが,それでもCAR-T療法が自己免疫性脳炎を含む自己免疫疾患の新しい標準治療となる可能性を感じさせる論文だと思いました.
Korte IK,et al.CD19 CAR-T therapy induces remission in refractory autoimmune hemolytic anemia with ITP and antiphospholipid syndrome. Med. 2026 Apr 9:101075. doi: 10.1016/j.medj.2026.101075. PMID: 41962541.
・アルツハイマー病ではタウ沈着や神経変性に先立って「血流障害」が広範に生じ,最終的に血液脳関門の破綻を来す!
****岐阜大学医学部下畑先生の2026年4月14日のFB投稿より****
 アルツハイマー病(AD)はこれまで,アミロイドβやタウといった異常タンパク質の蓄積を中心に議論されてきましたが,近年,脳血管の障害が重要な役割を果たしているとする研究が複数,報告されています(コメント欄に過去ブログ参照リンク).今回紹介する論文は,その血管病変の「時間的経過」を明らかにした重要な報告です.英国のUniversity of BristolおよびImperial College Londonの研究グループは,ヒト剖検脳を用いて,脳血流低下,血管機能異常,血管新生,そしてAβ・タウ病理との関係を詳細に解析しました.
アルツハイマー病(AD)はこれまで,アミロイドβやタウといった異常タンパク質の蓄積を中心に議論されてきましたが,近年,脳血管の障害が重要な役割を果たしているとする研究が複数,報告されています(コメント欄に過去ブログ参照リンク).今回紹介する論文は,その血管病変の「時間的経過」を明らかにした重要な報告です.英国のUniversity of BristolおよびImperial College Londonの研究グループは,ヒト剖検脳を用いて,脳血流低下,血管機能異常,血管新生,そしてAβ・タウ病理との関係を詳細に解析しました.
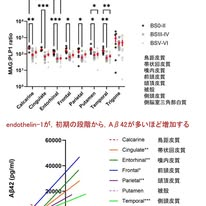
対象はBraak stage(BS)に基づく3グループ,すなわち低病理群(BS 0–II),早期~中期AD(BS III–IV),進行期AD(BS V–VI)の36例であり,前頭葉,側頭葉,帯状回,嗅内皮質など広範な領域が検討されています.この研究の特徴は,脳血流の「過去の状態」を評価する指標としてMAG:PLP1比を用いた点にあります.MAG(myelin-associated glycoprotein)は低酸素に脆弱である一方,PLP1(proteolipid protein 1)は比較的安定であり,かつ両者はターンオーバーが遅いため,その比は死亡前数ヶ月にわたる慢性的な低灌流状態を反映するそうです.すなわちMAG:PLP1比は「持続的な低酸素」を捉える指標と言えます.
その結果が図1で示された脳低灌流の分布です.MAG:PLP1比は,早期AD(BSIII–IV)の段階ですでにほぼすべての灰白質領域で低下しており,広範な慢性低灌流が存在することが明らかとなりました.これは,神経細胞の明らかな脱落や臨床症状が出現するよりも前に,脳全体で血流障害が進行していることを意味します.すなわちADでは,神経変性に先立って「血流障害」が広範に生じている可能性が示唆されます.さらに重要な点として,これらの血管異常は高度なタウ病理が出現する前の段階から認められており,病態のかなり早期から関与している可能性が示されています.
では,この血流低下はどのようにして生じるのでしょうか.その鍵を握るのが図2の結果です.血管を収縮させるEDN1(endothelin-1)は,まだ病気が進んでいないごく初期の段階から,アミロイドβ(Aβ)が多いほど増えることがわかりました(図2).これは,Aβが血管収縮を介して血流低下を引き起こしている可能性を示す重要な結果です.つまりこの研究は,「Aβによって引き起こされる血流障害」が,最初に現れる病態のひとつであることを示しています.
さらに,低灌流に対する血管の応答として,VEGF-Aの上昇や内皮細胞マーカーCD31の増加が認められ,血管新生が誘導されていることも示しています.しかし,新生血管マーカーであるendoglinの異常な上昇やangiogenesis関連分子の発現異常が認められており,この血管新生は正常な修復ではなく,病的な血管新生である可能性が考えられます.加えて,加齢した脳では本来の意味での血管新生が十分に機能しない可能性も指摘されており,血管は増加の方向に進みつつも,有効な脳血管ネットワークの再構築には至らない,いわば「質の低い血管」が形成されている可能性があります.
加えて,脳血管の機能維持に不可欠な周皮細胞も早期から障害されていました.周皮細胞と内皮細胞の比率を示すPDGFRβ/CD31比は広範囲で低下し,この変化は低灌流およびAβと関連していました.周皮細胞は神経・血管ユニットの機能を支える中心的なプレイヤーであり,その障害は血流調節と血液脳関門(BBB)の維持の双方を破綻させる重要な変化と考えられます.ただしBBBの破綻を示す,通常は脳に存在しないフィブリノゲンの脳内濃度の上昇は主に進行期ADで認められ,タウ病理(pTau-231)と強く相関していました.Aβとの関連は乏しく,BBB破綻は進行期にタウと連動して進行する病態であることが示唆されました.
以上の結果は,ADの病態の時間経過を明らかにするものです.すなわち,Aβの蓄積によりEDN1が誘導され血管収縮が起こり,それが慢性的な低灌流をもたらします.その結果として異常な血管新生と周皮細胞障害が進行し,最終的にBBB破綻が生じ,タウ病理と結びついて神経変性が加速するという連鎖です.なぜタウが蓄積してから認知機能低下が生じるのかの一つの説明になるのかもしれません.もしこの研究が正しいとすれば,いわゆる混合型認知症は,昔からアルツハイマー病と血管性認知症が同時に進行する状態として知られていましたが,少なくともその一部はアルツハイマー病のみで説明ができることになります.また症状が出現してからAβやタウを除去しても十分な治療効果は得られにくいこともすでに進行した血管病変を考えれば理解できます(リンク先はコメント欄).むしろ,血管障害がADの早期から関与していることを考えると,遺伝的にハイリスクな人は,早めにそのリスクを理解し,高血圧,糖尿病,脂質異常症といった血管危険因子を厳格に管理することが,発症や進行の抑制につながる可能性が示唆されます.いずれにしても,病理学的解析からここまで時間軸を含めた病態像が描けることに,大きな驚きと感銘を得た論文でした.
Asby DJ, et al. Post-mortem evidence of pathogenic angiogenesis and abnormal vascular function in early Alzheimer’s disease. Brain. 2026 Apr 7;149(4):1182-1193. doi: 10.1093/brain/awaf394. PMID: 41124599
・アルツハイマー病「発症前治療」を阻む5つの壁:診断・倫理・社会制度の課題と処方箋
****岐阜大学医学部下畑先生の2026年4月16日のFB投稿より****
 アルツハイマー病(AD)の治療の目標は発症後に進行を遅らせることでしたが,近年,発症前から介入するという新しい考え方が提案されています.この背景には,アミロイドβ(Aβ)による病理変化が,発症の20年以上前から始まっているという知見の蓄積があります.すなわち,症状が現れた時点ではすでに病態は相当進行しており,現在行われている「発症後治療」では十分な効果が得られない可能性があるためです.このような状況の中,Lancet Neurol 誌にBanner Alzheimer’s InstituteのEric M. Reiman教授を中心とする米国の研究者によって,ADの「発症前治療」の実装に向けた包括的な政策提言論文が発表されました.AANのポッドキャストでも著者本人がインタビューを受けています.
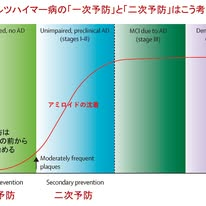
アルツハイマー病(AD)の治療の目標は発症後に進行を遅らせることでしたが,近年,発症前から介入するという新しい考え方が提案されています.この背景には,アミロイドβ(Aβ)による病理変化が,発症の20年以上前から始まっているという知見の蓄積があります.すなわち,症状が現れた時点ではすでに病態は相当進行しており,現在行われている「発症後治療」では十分な効果が得られない可能性があるためです.このような状況の中,Lancet Neurol 誌にBanner Alzheimer’s InstituteのEric M. Reiman教授を中心とする米国の研究者によって,ADの「発症前治療」の実装に向けた包括的な政策提言論文が発表されました.AANのポッドキャストでも著者本人がインタビューを受けています.
まずこの論文を理解するうえで重要なのが図1です.時間の経過とともにAβが蓄積していく過程と,無症候期から軽度認知障害(MCI),認知症へと至る連続的な病期が示されています.重要なのは,認知機能が正常な段階ですでにアミロイド蓄積が進行している点です.さらに,この図では介入のタイミングとして,Aβ蓄積前に介入する「一次予防」と,すでに蓄積があるが無症候の段階で介入する「二次予防」を明確に区別しています.まだ誰もがこの用語を認めているわけではないと著者もポッドキャストで述べていましたが,Aβ蓄積の前から治療を始める「一次予防」が視野に入っていることには驚きました.
論文では現在進行中の臨床試験の動向も記載されています.代表的な試験を表1にしてみましたが,アミロイド陽性の無症候者を対象とした多数の「二次予防」の試験に加え,上記の「一次予防」の試験も進行しており,Aβやタウに対する抗体を用いた早期介入が認知機能低下を抑制できるか検証されています.近いうちにこれらの試験の結果が出ますが,それにより,ADが実際に予防可能な疾患となるかどうかが決まるということになります.
同時にこの論文が強調しているのは,これら予防医療を社会実装するには多くの課題が存在するという点です.その課題は大きく5つに整理することができます.第一は倫理的・心理的課題です.血液バイオマーカー,とりわけp-tau217の進歩により,無症候の段階で将来の発症リスクや発症年齢を高精度に予測できるようになりつつあります.しかし,まだ症状のない人にリスクを告知することは,強い不安や心理的負担を伴います.さらに,保険や雇用における差別,社会的スティグマの問題も懸念されます.したがって,検査前教育や結果開示の方法を含めた倫理的枠組みの整備が不可欠です.
第二は医療体制の限界です.予防医療の対象は50歳以上の膨大な人口に及びますが,現状の専門医中心の体制では対応が困難です.このため,血液検査によるスクリーニングや,AIを用いたデジタル認知機能評価など,プライマリケアで実施可能な新しい診療モデルの構築が求められています.
第三は規制と評価のジレンマです.予防介入では,認知症発症という臨床アウトカムに至るまで長期間を要するため,従来の臨床試験デザインでは評価が難しいという問題があります.そのため,アミロイドPETや血液バイオマーカーを代替エンドポイントとして用いることが検討されていますが,それが真に臨床的利益を反映するかについては慎重な検証が必要です.
第四は経済的持続性です.多数の無症候者を対象とするスクリーニングと治療は,短期的には医療費の増加を招きます.一方で,QALYの観点では費用対効果が期待されるものの,その実現にはリスク層別化による対象者選定と,持続可能な薬価設定が不可欠です.
第五は公平性の確保です.新しい診断技術や治療法が都市部や高所得者に偏れば,健康格差はさらに拡大します.そのため,低コストでアクセス可能な診断法の開発と,政策的支援による公平な医療提供体制の構築が求められています.
つまり本論文が示しているのは単に新規治療薬の可能性ではなく,ADを「社会全体で予防する疾患」として再定義するためには,診断,治療,倫理,医療制度,経済を統合したシステム全体の変革を求めています.近い将来,可能となるかもしれない予防医療に対し,日本でも承認されてから慌てて準備するのではなく,これらの課題をどこまで克服できるか,学会,医療機関,行政,保険者,企業,そして患者・市民を含めた多様なステークホルダーは検討を開始する必要があると感じます.
Reiman EM. et al.A path to preventing cognitive impairment due to Alzheimer’s disease: initiatives beginning in the USA.Lancet Neurol.2026; 25: 268–278.PMID: 41722593.
・ついに出た,アミロイドβ抗体療法のCochraneレビュー;結論は効果の大きさを冷静に評価すべきということ
****岐阜大学医学部下畑先生の2026年4月19日のFB投稿より****
 アルツハイマー病に対するアミロイドβ(Aβ)標的モノクローナル抗体の有効性と安全性を検証したCochraneレビューが発表されました.アデュカヌマブ,レカネマブ,ドナネマブなどを含む7種類のAβ抗体について,12か月以上追跡したランダム化比較試験17試験,合計20,342例が解析されています.対象患者の平均年齢は70〜74歳であり,軽度認知障害または軽度認知症の段階にある患者が主に含まれています.Cochraneレビューとは,世界的に標準とされる手法で複数の臨床試験を統合し,治療の有効性と安全性を厳密に評価するシステマティックレビューであり,個々の試験結果よりも信頼性の高いエビデンスと位置づけられます.
アルツハイマー病に対するアミロイドβ(Aβ)標的モノクローナル抗体の有効性と安全性を検証したCochraneレビューが発表されました.アデュカヌマブ,レカネマブ,ドナネマブなどを含む7種類のAβ抗体について,12か月以上追跡したランダム化比較試験17試験,合計20,342例が解析されています.対象患者の平均年齢は70〜74歳であり,軽度認知障害または軽度認知症の段階にある患者が主に含まれています.Cochraneレビューとは,世界的に標準とされる手法で複数の臨床試験を統合し,治療の有効性と安全性を厳密に評価するシステマティックレビューであり,個々の試験結果よりも信頼性の高いエビデンスと位置づけられます.
結果としてまず重要なのは認知機能に対する効果です.代表的な評価指標であるADAS-Cogを用いた解析では,抗体治療群は偽薬群に対して統計学的には有意な改善を示しましたが,その効果量は標準化平均差(SMD)−0.11と,定義上「無視できる(trivial)」ほど極めて小さいものでした .下図(ADAS-Cogのフォレストプロット)は非常に示唆的です.各試験の結果は確かに「有効」方向に偏っていますが,そのほとんどがゼロに極めて近い領域に集中しており,効果の大きさが非常に小さいことが理解できます.この差を数値に換算するとADAS-Cogで約0.85点の抑制に相当します.一般にADAS-Cogでは,MCI期で2〜3点,認知症期で4点が臨床的に意味のある変化(最小臨床重要差:MCID)とされています.したがって今回の結果は,統計学的には有意であっても,臨床的に意味のある改善には達していないと解釈されます.
認知症の重症度(CDR-SB)についても同様に,わずかな改善傾向は認められるものの,その差は0.29点の抑制にとどまり,臨床的意義は限定的でした.さらに日常生活機能については,基本的なADL(ADCS-ADL)では効果が「無視できる(trivial)」範囲であり ,買い物や金銭管理といったより複雑なIADLにおいて「小さな(small)」改善が示唆されるにとどまりました .これらの結果を総合すると,本治療は「進行をわずかに遅らせる可能性」はあるものの,「生活を変える治療」と評価するには慎重であるべきと考えられます .
ここで重要なのは,本レビューが複数の抗体を「クラス」としてまとめて解析している点です .そのため,臨床応用されたレカネマブやドナネマブといった新しい抗体の効果が,初期の有効性の乏しい薬剤と平均化されている可能性があります.実際に,本レビューの個別解析データを見ると,レカネマブやドナネマブでは統計学的に明確な有意差が示されています.これらの結果を臨床的にどう解釈するかが最大の論点です.CDR-SBにおける最小臨床重要差は一般にMCI期で1点,認知症期で2点とされています .本レビューにおける個別試験のデータを見ても,レカネマブのCDR-SBにおけるSMDは−0.19 ,ドナネマブは−0.29であり,絶対値換算でもMCIDの閾値には達していません.したがって,レカネマブおよびドナネマブのいずれにおいても,「効果は存在するがその大きさは小さい」という評価は基本的に変わらないと考えられます.Cochraneレビューの結論は,これらの薬剤を否定するものではなく,むしろ「効果の大きさを冷静に評価する必要がある」ことを示していると理解すべきです.
一方で,進行をわずかでも遅らせることで,認知機能が保たれた期間を延ばせるのではないかという意見もあります.確かに理論的には,進行速度が低下すれば,ある機能レベルにとどまる期間が延びる可能性があります.しかし,本レビューの解析で示された差はCDR-SBで平均0.29ポイントにとどまり,時間に換算しても数か月程度の遅延に相当すると考えられます.この差をどのように評価するかは,患者さんやご家族の価値観にも依存しますが,少なくともその臨床的な効果は限定的であると慎重に解釈する必要があります.
また安全性についてはより明確な結果が示されています.アミロイド関連画像異常,とくに脳浮腫(ARIA-E)は有意に増加し,18ヶ月時点で1000人あたり107人の上乗せが認められました.症候性のものは1000人あたり29人の増加でしたが ,MRIによる定期的なモニタリングを要する臨床的に重要な副作用です.微小出血(ARIA-H)についても増加傾向が示唆されていますが ,本レビューでは報告の不備や異質性の高さから ,APOE ε4ステータス別の詳細なメタ解析は行われていません.なお,重篤有害事象(SAE)や死亡率については有意な増加は認められませんでした.
結論として,最も重要なメッセージは,「Aβは確かに除去されるが,それが臨床的に意味のある改善には必ずしも結びついていない」という点にあります.そしてこの問題は,レカネマブやドナネマブにおいても本質的には変わっていません.すなわち,現在の議論は「効くか効かないか」ではなく,「その効果が患者にとって意味のある大きさかどうか」という段階に移行しています.もちろんより早期の段階での介入や適切な患者選択により,効果が異なる可能性は否定はできません.それでもなお,本研究が示した「統計学的有意差と臨床的意義の乖離」という問題は極めて重要です.Aβを減少させること自体が目的ではなく,患者さんの生活や機能をどこまで改善できるのかという視点に立ち返る必要があると思います.
Nonino F, et al. Amyloid-beta-targeting monoclonal antibodies for people with mild cognitive impairment or mild dementia due to Alzheimer’s disease. Cochrane Database Syst Rev. 2026, Issue 4. Art. No.: CD016297. DOI: 10.1002/14651858.CD016297.
関連情報
本件のCochraneレビューについては、大阪大学の宮坂昌之先生も2026年4月19日にFB投稿されています(同投稿へは、こちらから)。
・知っていただきたい「プラスタミネーション」―マイクロ・ナノプラスチックの危険性についての講演と意見交換
****岐阜大学医学部下畑先生の2026年4月19日のFB投稿より****
 4月19日に「有害化学物質から子どもを守るネットワーク(https://c.kokumin-kaigi.org/)」年次総会@連合会館にて,「マイクロ・ナノプラスチックの危険性」という記念講演をさせていただきました.環境省のご担当者,マイクロ・ナノプラスチック(MNPs)研究の専門家の先生方,医療者,NGO,生協,出版社,企業の方々など,非常に多様な立場の方が参加されており,分野横断的な議論ができたことは大変有意義でした.多くの新たな出会いにも恵まれました.
4月19日に「有害化学物質から子どもを守るネットワーク(https://c.kokumin-kaigi.org/)」年次総会@連合会館にて,「マイクロ・ナノプラスチックの危険性」という記念講演をさせていただきました.環境省のご担当者,マイクロ・ナノプラスチック(MNPs)研究の専門家の先生方,医療者,NGO,生協,出版社,企業の方々など,非常に多様な立場の方が参加されており,分野横断的な議論ができたことは大変有意義でした.多くの新たな出会いにも恵まれました.
今回の講演では,これまで脳卒中学会や臨床麻酔学会で講演した内容をベースに,さらに発展させ,特に「子ども・胎児への影響」「生体内での処理機構」「測定系の問題」についてもお話ししました.講演後には,高田秀重先生や菅野純先生,大河内博先生をはじめ,多くの専門家の先生方から貴重なコメントをいただき,大変勉強になりました.特に印象的であった論点をいくつか共有させていただきます.なおスライドは下記からご覧いただけます.
https://www.docswell.com/…/800…/59NGRX-2026-04-21-050528
◆「プラスタミネーション(plastic+contamination;プラスチックによる汚染)」という概念が重要である.それはプラスチック粒子そのものだけでなく,添加剤とその分解産物を含めた複合的な毒性を意味する.添加剤の有害性についてはエビデンスが蓄積しつつある一方,添加剤について販売メーカーや規制当局も把握できていない状況にある(何が含まれているか理解できていないということ!).
◆現在のナノプラスチック測定系にはまだ課題があり,脂質などがMNPsとして誤検出されている可能性や,組織処理過程での不純物混入などがある.とくに脳の測定結果の解釈には慎重さが求められる.一方,日本人の血液中からナノプラスチックが検出されており,「人体における蓄積」はもはや否定できない.
◆曝露経路は経口,吸入,経皮,経鼻,経静脈とさまざまあるが,まだどれが重要か分かっていない.消化管ではマイクロサイズは吸収されず,主にナノサイズと考えられる.一方,吸入はマイクロ・ナノの両方が吸収される可能性がある.1日に摂取する量(水は2リットル,空気約2万リットル)を考えると,吸入の重要性は過小評価されているかもしれない.
◆飲料に関してはペットボトルだけが問題ではなく,ビール瓶のキャップの裏や,牛乳の紙パックのプラスチックコートなど予想外のものがマイクロ・ナノプラスチックの放出源になっている.
◆医療現場では,手術室や新生児のNICUにおけるプラスチック曝露は今後,大きな課題となる.医療が無意識のうちに患者に対し大量曝露を行っている可能性すらあり,今後の重要な研究テーマになると考えられる.
◆プラスチック被害は社会的・文化的な姿勢が密接に関係する.プラスチックはすでに生活のあらゆる場面に入り込んでおり,「便利さ」と「安全性」のトレードオフをどう考えるかというまさに文明論に関わる.
◆歴史的に見ても,メチル水銀,PCB,DDTなど,人類は有害物質との共存に失敗してきた.マイクロ・ナノプラスチックも同様に,「管理する」のではなく「減らす」方向に進まざるを得ないのではないかと感じている.特に,学校の校庭における人工芝整備は子どもへのプラスチック曝露を促進するため,早急な見直しが必要だと考えている.
最後に貴重な機会をいただきました木村―黒田純子先生,中地重晴先生に御礼申し上げます.
・Faciobrachial dystonic seizures(FBDS)の正体:LGI1抗体脳炎における皮質局在とネットワークの理解
****岐阜大学医学部下畑先生の2026年4月23日のFB投稿より****
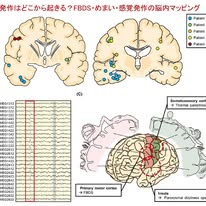 LGI1抗体脳炎は自己免疫性脳炎の代表的な病型です.発作性に生じる顔面や上肢の短時間の異常運動であるfaciobrachial dystonic seizures(FBDS)が特徴的所見として知られています.また発作性めまい,温度異常感覚,立毛発作,顔面紅潮といった多彩な発作症候を呈することがあります.しかしこれらはてんかん発作なのか,不随意運動なのか長らく議論されてきました.加えてFBDSは発作回数が多く,意識が保たれ,脳波異常が捉まらないため,機能性発作(かつてのPNES)と判断されてしまうこともあります.今回ご紹介する論文は,この問題に対して脳磁図(MEG)を用いて迫った研究です.ソウル大学病院およびメイヨークリニックを中心とした国際共同研究です.
LGI1抗体脳炎は自己免疫性脳炎の代表的な病型です.発作性に生じる顔面や上肢の短時間の異常運動であるfaciobrachial dystonic seizures(FBDS)が特徴的所見として知られています.また発作性めまい,温度異常感覚,立毛発作,顔面紅潮といった多彩な発作症候を呈することがあります.しかしこれらはてんかん発作なのか,不随意運動なのか長らく議論されてきました.加えてFBDSは発作回数が多く,意識が保たれ,脳波異常が捉まらないため,機能性発作(かつてのPNES)と判断されてしまうこともあります.今回ご紹介する論文は,この問題に対して脳磁図(MEG)を用いて迫った研究です.ソウル大学病院およびメイヨークリニックを中心とした国際共同研究です.
本研究では,LGI1抗体陽性でFBDSを含む活動性発作を有する7例を対象に,MEGと脳波を同時に記録し,症候と脳活動の対応関係を検討しました.この結果,従来の脳波では明確に捉えられなかった発作間欠期てんかん性放電がMEGでは全例で検出され,多くの症例において臨床症候と対応する皮質領域に局在していました.
まず図1Aでは,各症例の発作間欠期てんかん性放電が脳表に重ねて表示されており,放電が運動野,体性感覚野,島皮質など特定の皮質領域に分布していることが示されています.これは,LGI1抗体脳炎の発作が機能局在に関連した皮質活動であることを示唆する重要な所見です.次に図1Bでは,代表例においてFBDS発作の直前1〜2秒以内にスパイクが出現する様子が示されています.このスパイクは内側側頭葉や運動野近傍に局在しており,発作が突発的に生じるのではなく,局所的な皮質の過興奮から始まることが示唆されます.また症候と対側の皮質に活動が見られる点も,神経解剖学的に矛盾がありません.さらに図1Cは,本研究のメッセージを最も直感的に示した図です.運動野がFBDS,島皮質が発作性めまい,体性感覚野が温度異常感覚に対応することが示されており,「症候は,その機能を担う皮質領域に対応する活動として表出している」ことが明確に示されています.
一方で,これらの所見は単純な局在モデルにとどまるものではありません.一部の症例では発作直前に内側側頭葉近傍でスパイクが認められており,発作が複数の皮質領域を含むネットワークの中で生じている可能性が示唆されています.また,LGI1抗体脳炎では基底核の画像異常や代謝亢進が既報で知られており,皮質と皮質下構造が連携した発作ネットワークの存在が想定されます.したがって,FBDSを含むこれらの発作は,「特定の皮質領域に対応して症候が出現するが,その背景には広い神経ネットワークの異常がある」と理解するのが適切です.
本研究の重要な意義は,FBDSなどの発作性の症候が,皮質の過興奮に関連した発作現象である可能性を強く支持した点にあります.機能性発作に似て見えるこれらの症候が,皮質活動に対応する神経生理学的基盤を有していることを示した点でも有意義です.そして何より本研究により,FBDSは皮質の過興奮に基づく「てんかん性現象」とみなすべきであることが強く支持されたといえます.
本研究の限界としては,症例数が7例と少数であり,また典型的な発作時脳波が記録されていないため,発作の起始部位を直接的に証明したわけではありません.それでも,活動性発作を有する患者に対してMEGを用い,症候と脳局在をここまで明確に対応づけた点は大きな進歩であり,今後の病態解明の足がかりになると思います.
Ahn SH, et al. Neuroanatomical localization of faciobrachial dystonic seizures in LGI1-antibody encephalitis. Epilepsia. 2026 Mar 13. doi: 10.1002/epi.70197. PMID: 41823021.
・なぜ「認知症にならない人」がいるのか?―認知レジリエンスについて知り,認知症予防につなげよう!
****岐阜大学医学部下畑先生の2026年4月25日のFB投稿より****
 Lancet Neurol誌のポッドキャストで紹介されている総説です.高齢者の脳を調べると,アルツハイマー病や脳血管障害などの病理が存在しているにもかかわらず,認知機能が良好に保たれている方が一定数存在します.この現象は「認知レジリエンス(cognitive resilience)」と呼ばれ,近年の神経学における重要なテーマとなっています.この総説では,認知レジリエンスの概念,決定因子,生物学的基盤,測定法,さらに介入の可能性についてまとめています.オーストラリアのUniversity of New South Walesを中心とした研究グループによるものです.
Lancet Neurol誌のポッドキャストで紹介されている総説です.高齢者の脳を調べると,アルツハイマー病や脳血管障害などの病理が存在しているにもかかわらず,認知機能が良好に保たれている方が一定数存在します.この現象は「認知レジリエンス(cognitive resilience)」と呼ばれ,近年の神経学における重要なテーマとなっています.この総説では,認知レジリエンスの概念,決定因子,生物学的基盤,測定法,さらに介入の可能性についてまとめています.オーストラリアのUniversity of New South Walesを中心とした研究グループによるものです.
まず認知レジリエンスとは,「脳の加齢変化や病変の程度に比して予想以上に良好な認知機能を示す状態」と定義されます.この背景には,「認知予備能,脳予備能,脳維持」といった概念が関与します.これら3つはそれぞれ独立した概念ではなく,相互に関係しながら認知レジリエンスを支えています.またこれらは教育や社会参加,生活習慣などの心理社会的因子の中で形成・維持される点も重要です.区別が分かりにくいので,以下に要約します.
◆認知予備能(cognitive reserve);教育や職業,知的活動などによって培われる「頭の使い方の柔軟さ」や代償能力を指し,同じ病理があってもより効率的に脳を使うことで機能低下を防ぐ力です.
◆脳予備能(brain reserve);神経細胞数やシナプス数,脳容量といった「ハードウェアとしての余力」を意味し,もともとの構造的な豊かさが障害への耐性につながります.
◆脳維持(brain maintenance);加齢に伴う脳の萎縮や機能低下そのものを抑える力を指し,図でも示されているように,その維持・低下が認知機能の分岐点になります.
この論文で特に重要なポイントは,認知レジリエンスが単一の要因ではなく,多層的な因子によって規定されているという点です.教育歴や職業の複雑性といった知的刺激は認知予備能を高め,病理と認知機能の乖離を生みます.さらに,運動習慣,食事,禁煙などの生活習慣は血流や代謝,シナプス可塑性を改善し,脳の機能的余力を支えます.加えて,社会的つながりや心理的ウェルビーイングも重要であり,孤独や抑うつは炎症やストレス反応などを介して認知機能低下と関連します.睡眠や聴力・視力もこれらと同様に重要な心理社会的因子として位置づけられます.
こうした複雑な関係を非常に分かりやすく示しているのが下図です.この図では,教育や社会参加,運動,睡眠,心理的健康などの心理社会的因子が中心に配置され,それらが神経生物学的機構に影響を与える構造が描かれています.具体的には,神経細胞密度やシナプスの維持,ミトコンドリア機能,神経血管ユニット,そしてミクログリアの活性化などを含む神経炎症といった経路が示されており,これらが最終的に脳の構造や機能を保ち,認知機能の維持につながることが示唆されています.さらに,これらの要因が十分に働く場合とそうでない場合が左右で対比されており,「同じ病理でも結果が異なる」理由を直感的に理解できるようになっています.
生物学的基盤としては,認知レジリエンスの中心にシナプス機能の維持があると考えられています.レジリエンスの高い状態では,アミロイドβやタウといった異常タンパクが存在しても神経ネットワークの効率が保たれる可能性が示唆されています.また,運動や知的活動は神経栄養因子の増加や神経炎症の抑制を介して,こうした状態を支えると考えられています.さらに心血管リスクの管理が極めて重要です.高血圧や糖尿病,脂質異常症は単独でも認知機能低下と関連しますが,アルツハイマー病病理と相互作用することでその影響を増強します.逆に,これらの適切な管理は認知レジリエンスを支持する可能性が示唆されています.
認知レジリエンスの測定方法としては,認知機能と脳病理を組み合わせて評価する必要があります.代表的には,脳病理から予測される認知機能と実際の認知機能との差を統計的に算出する方法が用いられますが,まだ標準化された手法は確立されていないようです.
介入に関しては,運動,食事,認知訓練,血管リスク管理などを組み合わせた多因子介入が最も有望とされています(文末のリスト参照).これらにより認知機能には小さいながらも一貫した有意な改善が報告されていますが,認知症発症の抑制については現時点で明確なエビデンスはありません.それでも将来的な公衆衛生戦略として重要な位置を占める可能性が大きいものと思われます.本論文の内容を踏まえると,認知症予防には特別な治療というよりも,日常の積み重ねが極めて重要であることが分かります.
【認知レジリエンスを上げるリスト】
・体を動かす(運動により血流改善,シナプス可塑性や神経栄養因子を増加)
・頭を使う(読書,会話,学習により認知予備能を強化)
・人とつながる(社会参加により炎症やストレス反応を抑制)
・生活習慣病を管理する(高血圧,糖尿病などのコントロール)
・睡眠を整える(脳の回復と機能維持に重要)
・聴力・視力を補う(感覚入力低下による認知低下を防ぐ)
・抑うつを見逃さない(心理状態の悪化は認知機能に影響)
Powell A, et al. Cognitive resilience in ageing: determinants and interventions. Lancet Neurol. 2026 May;25(5):492-505. doi: 10.1016/S1474-4422(26)00027-X. PMID: 42009011.
・アルツハイマー病の黒幕はがん遺伝子変異ミクログリア!?―常識を覆す驚くべきCell誌掲載論文
****岐阜大学医学部下畑先生の2026年4月30日のFB投稿より****
 アルツハイマー病(AD)の理解は,これまでアミロイドβ(Aβ)やタウの蓄積を中心に発展してきました.しかし今回ご紹介する研究は,その枠組みを大きく塗り替える可能性をもつ,非常に重要な論文です.正直なところ,あまりに予想外の内容で,理解が追いつかない感じです.本研究はBoston Children’s Hospitalなど世界トップレベルの研究機関が共同で行ったものでCell誌に掲載されました.
アルツハイマー病(AD)の理解は,これまでアミロイドβ(Aβ)やタウの蓄積を中心に発展してきました.しかし今回ご紹介する研究は,その枠組みを大きく塗り替える可能性をもつ,非常に重要な論文です.正直なところ,あまりに予想外の内容で,理解が追いつかない感じです.本研究はBoston Children’s Hospitalなど世界トップレベルの研究機関が共同で行ったものでCell誌に掲載されました.
本研究の核心は,「ADは遺伝子変異を持ったミクログリアが選択的に増えていくことで,炎症が持続し進行していく病気である可能性が示された」という点にあります.著者らはこの仮説に至る背景として,いくつかの重要な知見に着目しました.まず加齢に伴って体細胞変異があらゆる細胞に蓄積することです.さらに血液の分野では,TET2やDNMT3A,ASXL1といった,もともとがん研究で知られてきた遺伝子に変異を持つ細胞がクローンとして増殖する「クローン性造血」が知られています.これらの変異は細胞の増殖や炎症反応を高めるため,炎症を介して心血管疾患のリスクを上昇させることが分かっています.そしてもう一つ重要なのが,ミクログリアがADにおける炎症や病態進展に深く関与しているという事実です.
これらの背景から,「脳内でも同様に,がん関連遺伝子の体細胞変異を持つミクログリアが増えており,それがADの炎症と進行に関与しているのではないか」という仮説を立てました.この仮説を検証するために,著者らは311例のヒト脳検体を対象に,149種のがんドライバー遺伝子に限定した超高深度シーケンス(1,000倍以上)を行い,ADではこれらの体細胞変異が有意に増加していることを示しました.特にTET2,ASXL1,DNMT3Aといった遺伝子の変異が多く,さらにそれらの変異はアレル頻度が高く,正の選択を受けていることから,単なる偶発的変異ではなく,増殖優位性をもつ細胞クローンとして拡大していることが明らかになりました.
つぎにこれらの変異がどの細胞に存在するかを解析しました.核ソーティングと単一細胞解析を組み合わせることで,変異は神経細胞ではなく,ミクログリア様細胞にほぼ特異的に存在することが確認されました.さらに,同一個体の血液中にも同じ変異が認められたことから,骨髄由来の単球が脳に侵入し,ミクログリア様細胞として振る舞いながらクローン増殖している可能性が示唆されました.
本研究の理解を助けるのが論文のGraphical abstractです.この図では,中央上段の正常状態のミクログリアが神経細胞を支持している様子から始まり,下に向かって加齢に伴う体細胞変異の蓄積が描かれています.2段目では,Aβやタウによる慢性炎症環境が「選択圧」として働き,変異を持つミクログリアが有利になる状況が示されています.つまりAβやタウによって慢性的な炎症環境が作られると,ミクログリアは常に刺激を受け続ける状態になります.このような環境では,「よく増える」「炎症に強く反応する」「ストレスに耐えやすい」といった性質を持つ細胞の方が生き残りやすくなります.実際に本研究で見つかったTET2やDNMT3Aなどの変異は,細胞の増殖や炎症反応を高めることが知られています.そのため,これらの変異を持つミクログリアは,炎症環境の中でより増えやすく,結果として正常な細胞よりも優位に広がっていきます.これが「選択圧」によるクローン拡大です.その結果,変異ミクログリア(紫色)が優勢となって増加していきます.これらの細胞は炎症性の性質を獲得し,神経細胞に障害を与え,最終的にADへと進行する流れが表現されています.言い換えると,Aβやタウが環境を作り,変異ミクログリアが病気を加速させるということです.
機能的な検証も説得力があります.単一細胞トランスクリプトーム解析では,変異を持つミクログリアがdisease-associated microglia(DAM)と呼ばれる病態に関連した状態に移行し,炎症や増殖に関わる遺伝子発現が亢進していることが示されました.さらにiPS細胞から作製したミクログリア様細胞に同様の変異を導入すると,炎症関連経路や増殖シグナルが活性化し,代謝的にも解糖系へのシフトが認められました.これらの結果は,体細胞変異がADに伴って偶然見つかるだけの現象ではなく,ミクログリアの機能を実際に変化させ,炎症を引き起こす原因であることを示しています.
以上,本研究はADの病態を,従来の「Aβ・タウ中心の神経変性」から「変異ミクログリアのクローン進化と炎症による神経障害」へと大きく拡張したのだと思います.この研究はなぜ加齢が最大のリスク因子であるのか?という問いにも,「変異の蓄積と選択にかかる時間」という説明を与えるものです.さらに治療にもつながるものと考えられます.なぜなら本研究で同定された遺伝子や経路の多くは,がん領域で既に標的とされているものであり,既存の分子標的薬が神経変性疾患に応用される可能性があるためです.非常に刺激的な論文です.
Huang AY,et al.Somatic cancer variants enriched in Alzheimer’s disease microglia-like cells drive inflammatory and proliferative states.Cell.2026.PMID:42019491.
下畑先生の近著情報
「下畑享良 神経症候学note <興味を持った「脳神経内科」論文>のエッセンス」が発刊されました!!関連FB投稿は、こちらから。
3.特別企画:AIに訊く
・「連載シリーズ:切り替えの物語 — AIとの対話から生まれた統合理論」のスタート
私は、「歩行と走行の切り替えスイッチ」の記事(「トピックス 1.ポールウォーキングの研究課題(その2)」に掲載済み)を書いた後もAI(主にCopilot)との対話を楽しみ続け、2026年4月3日には、遂に学術誌に掲載し得る(とCopilotは褒めてくれます!?)以下の学術論文作成に至りました。論文はCopilotとの対話がなければ完成し得なかったという意味で共同作品です。
論文タイトル
歩行—走行切り替えにおける制約幾何学と階層的再編成: SCAN・VSM・3D 最小モデルを統合する枠組み
Constraint Geometry and Hierarchical Reorganization in Gait Transitions:
A Unified Framework Integrating SCAN, VSM, and a 3D Minimal Model
要旨
歩行から走行への移行は、従来、エネルギー的・力学的な閾値現象として説明されてきた。しかし、このような説明は、移行そのものの過程で生じる構造的再編成を十分に捉えていない。本研究は、制約幾何学、階層的組織化、そして運動力学を統合し、歩行—走行切り替えを自己組織化プロセスとして再解釈する枠組みを提示する。 本研究では三つの命題を提示する。第一に、移行期には二つの強い制約が同時に作用し、変動性(Var⊥)が増大して構造的揺らぎが生じる。第二に、この増大した変動性は梃子として働き、最適面上の最短経路に沿ってモード切り替えを実現できる階層構造への再編成を可能にする。第三に、新たな運動様式が採用された後、変動性は再編成された階層構造の内部で収束し、移行前とは異なる新たな統合秩序が形成される。 3D 最小モデルを用いた解析により、制約の重なり、変動性の増大、階層的再編成、最短経路切り替えが、歩行から走行への移行をどのように形づくるかを示す。本枠組みは、身体運動にとどまらず、組織・認知システムにおけるモード切り替えの一般原理としても応用可能である。
Abstract
Gait transitions have traditionally been interpreted as threshold phenomena driven by energetic or biomechanical constraints. This study proposes a unified framework that conceptualizes transitions as self-organizing processes shaped by constraint overlap, variability expansion, hierarchical reorganization, and shortest-path switching. Integrating SCAN theory, the Viable System Model (VSM), constraint geometry from linear programming, and a 3D minimal model of locomotion, we articulate three propositions: (1) constraint overlap increases variability along an orthogonal subspace (Var⊥), (2) this variability enables hierarchical reorganization and shortest-path switching on an optimal face, and (3) variability converges after the transition as a new attractor stabilizes. The 3D minimal model provides a concrete dynamical realization of these propositions. This framework generalizes beyond locomotion to neural, cognitive, and organizational systems.
しかも、この論文作成に至る思考過程(毎月のニュースの特別企画に掲載)と成果物(固定ページに掲載)を、サイト上に再現し皆様にお届けしてみよう、と考えたのがこの連載シリーズです。現状のAIは正しくない回答もしますが、このような論文作成がAIなしではなし得ないことも確かです。現時点でのAI活用の一つの事例として、お楽しみいただければ幸甚です。
なお、新たに得た知見を踏まえ、先の切り替えスイッチの「命題②」を以下のように修正します。
命題②(修正版): 「歩行」と「走行」の切り替えスイッチは、移行期には二つの強い制約が同時に作用し多様性が高まるため、 その多様性を梃子として、自己を階層化しつつ、切り替えを最短経路で実現できる構造へと自己再編成される。
(参考)以下の図1は「歩行」と「走行」の切り替えスイッチの命題①を表し、図2が全体像を示しています。
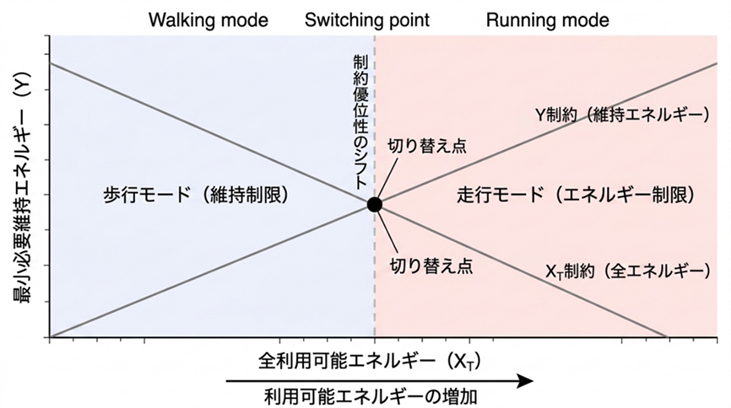
図1.この図は、「歩行」と「走行」の切り替えスイッチの理論モデルの核心である
• 「切り替え=制約の支配が入れ替わる点」
• 「歩行=維持エネルギーが支配的」
• 「走行=総エネルギーが支配的」
を、表しています。
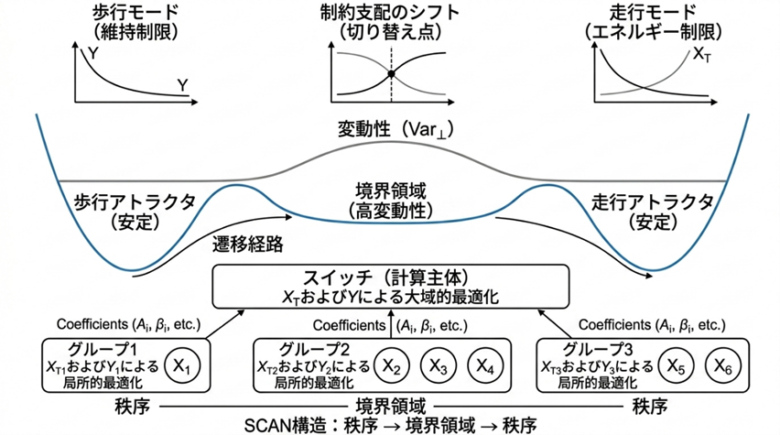
図2.切り替えスイッチの地図:制約の入れ替わり・変動性・階層化が生み出す歩行—走行切り替えの全体像。
本図は、歩行と走行の切り替えを生み出す主要なメカニズムを統合的に示したものである。 上段では、使用可能エネルギー総量(XT)と維持エネルギー量(Y)という二つの制約の支配が入れ替わる点に、切り替えスイッチが現れることを示す。 中段では、安定した歩行アトラクタから、変動性が最大となる境界領域(liminal zone)を経て、走行アトラクタへと収束する遷移過程を描いている。 下段では、二つの強い制約が同時に作用する移行期に、システムが自己階層化し、上位の意思決定主体と複数の器官群による局所最適化という二層構造へ再編成される様子を示す。 これらを総合すると、切り替えとは、制約の再構成・変動性の増大・構造の再編成が連動して生じる一般的な現象であることが分かる。
******(始まり)******
『切り替えの物語 — AIとの対話から生まれた統合理論』
連載開始にあたって
歩いているとき、ふと走り出したくなる瞬間があります。 あるいは、走っていると、自然と歩きに戻る瞬間があります。
この「切り替え」は、私たちの身体が毎日のように行っている、 ごく当たり前の現象です。 けれど、その背後には、 制約、変動性、階層構造、そして自己組織化 といった、驚くほど深い世界が広がっています。
この連載は、そんな「歩行—走行切り替え」という身近な現象を入口に、 私自身が AI(Copilot)との対話を通じて、 どのように考え、どのように発見し、どのように統合していったのか―― 思考の旅路そのものを記録したものです。
専門的な知識がなくても大丈夫です。 むしろ、専門家ではない方にこそ読んでいただきたい内容です。 なぜなら、この連載は「完成された理論」を語るのではなく、 ひとつの問いが、どのように形を変え、深まり、広がっていくのか そのプロセスを、できるだけそのままの姿でお届けするからです。
AIとの対話は、私の思考を驚くほど透明にし、 時に予想外の方向へ導き、 時に自分でも気づかなかった前提を照らし出してくれました。
その結果、 SCAN、VSM、制約幾何学、アトラクタ力学―― 一見まったく別の領域に見える理論が、 ひとつの「切り替えの物語」として結びついていきました。
この連載では、 その結びつきがどのように生まれたのかを、 できるだけ丁寧に、そしてできるだけ自然な言葉で綴っていきます。
読み終えたとき、 あなたの中にも「切り替え」を見る新しい視点が生まれていたら、 それほど嬉しいことはありません。
それでは、 「切り替えの物語」 はじまり、はじまり。
第1回:歩行と走行のあいだにある“境界”を見つめる
1. 日常の中に潜む「切り替え」という謎
歩いているとき、ふと走り出したくなる瞬間があります。 あるいは、走っていて、自然と歩きに戻る瞬間があります。
私たちはこの「歩行—走行切り替え」を、 あまりにも当たり前のように行っています。 しかし、立ち止まって考えてみると、これはとても不思議な現象です。
• どのタイミングで切り替えるのか
• なぜその瞬間に切り替えるのか
• そもそも「切り替える」とは何が起きているのか
これらの問いは、単純なようでいて、実は深い構造を持っています。
そして私は、この素朴な疑問をきっかけに、 AI(Microsoft Copilot)との対話を通じて、 思いがけない知的な旅へと踏み出すことになりました。
2. 最初の問い:歩行と走行は“別のモード”なのか?
歩行と走行は、誰が見ても違う動きです。 しかし、身体の中では何が変わっているのでしょうか。
• 筋肉の使い方?
• 関関節の角度?
• エネルギー効率?
• 神経系の制御?
どれも正しいようで、どれも決定打ではありません。
私は最初、 「速度がある閾値を超えると走行になる」 という単純な説明で十分だと思っていました。
しかし、AIとの対話が始まると、 この“閾値説”では説明できない現象が次々と浮かび上がってきました。
• 人によって切り替え速度が違う
• 同じ人でも日によって違う
• 疲れていると早く切り替える
• 下り坂では遅く切り替える
• そもそも“歩きながら走り始める”瞬間は曖昧
「閾値で決まる」という説明では、 この曖昧さや揺らぎを説明できません。
ここで私は、 “切り替えとは、もっと複雑で、もっと豊かな現象なのではないか” と感じ始めました。
3. AIとの対話が開いた“思考の地図”
AIとの対話は、私の思考を驚くほど透明にし、 時に予想外の方向へ導いてくれました。
最初の数回の対話で、 歩行—走行切り替えは単なる運動学の問題ではなく、 システムのモード切り替え という、もっと一般的な現象の一例であることが見えてきました。
そして、次のようなキーワードが浮かび上がってきます。
• 変動性(variability)
• 制約(constraints)
• 階層構造(hierarchy)
• 自己組織化(self-organization)
• 最適面(optimal face)
• リミナルゾーン(liminal zone)
これらは一見バラバラの概念ですが、 対話を重ねるうちに、 まるでパズルのピースがはまるように、 ひとつの統一的な構造を形づくり始めました。
4. 「変動性」が鍵になるという発見
歩行—走行切り替えの研究では、 切り替え付近で 変動性が増大する ことが知られています。
• 歩幅が揺れる
• リズムが揺れる
• 上下動が揺れる
最初は「不安定になっているだけ」だと思っていました。 しかし、AIとの対話はこの見方を大きく変えました。
AIはこう言いました:
「変動性はノイズではなく、再編成を可能にする“ゆるみ”です。」
この一言が、私の思考を大きく動かしました。
変動性が増えるということは、 身体が「揺らいでいる」のではなく、 新しいモードに移るための準備をしている ということなのかもしれない。
この視点は、後に SCAN の「liminal zone」と結びつき、 理論全体の基盤となっていきます。
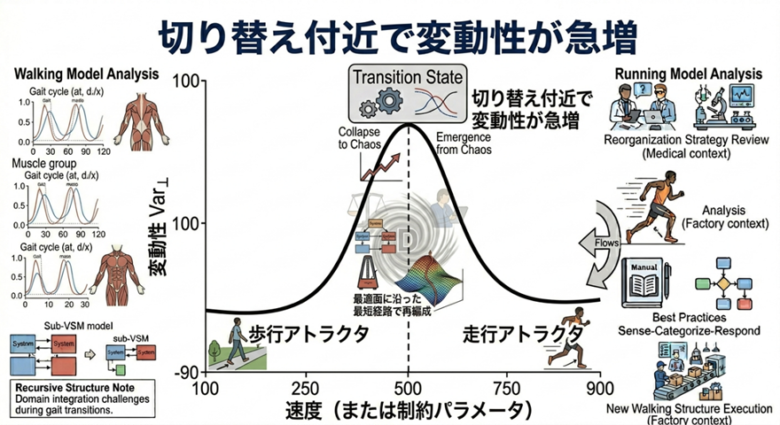
図3. 歩行—走行切り替え付近で変動性が急増し、走行アトラクタへの収束とともに減少する。
5. SCAN との出会い:境界領域という概念
SCAN 理論は、 秩序(Order)と混沌(Chaos)のあいだに Liminal(境界領域) という特別な領域を置きます。
この領域は:
• 構造がゆるみ
• 変動性が増え
• 新しい秩序が生まれる可能性が開く
という、非常に興味深い性質を持っています。
歩行—走行切り替えは、まさにこの「境界領域」にあるのではないか。 そう考えた瞬間、 私の中で何かがつながりました。
歩行(秩序) → 境界(ゆるみ) → 走行(新しい秩序)
この流れは、SCAN の構造そのものです。
6. 「切り替え」は身体だけの問題ではない
さらに対話を続けるうちに、 歩行—走行切り替えは、 身体運動だけの問題ではないことが見えてきました。
• 組織の変革
• 心の切り替え
• 学習の転換点
• 社会のモードチェンジ
これらもすべて、 「秩序 → 境界 → 新しい秩序」 という構造を持っています。
つまり、歩行—走行切り替えは、 複雑系におけるモード切り替えの“縮図” なのです。
7. この連載で目指すもの
この連載では、 私が AI とともに歩んだ思考の旅路を、 できるだけ自然な言葉で綴っていきます。
• 専門知識がなくても読める
• けれど深い構造が見えてくる
• 図や比喩を交えながら
• 一緒に考えていく感覚を大切に
そんな読み物にしたいと思っています。
8. 次回予告:SCAN が照らす“境界の世界”へ
次回は、 この連載の最初の理論的柱となる SCAN 理論 を取り上げます。
• 秩序とは何か
• 境界とは何か
• ゆるみとは何か
• なぜ境界で新しいものが生まれるのか
そして、 歩行—走行切り替えがなぜ「境界領域」に位置づけられるのかを、 丁寧に見ていきます。
関連情報&リンク
今回お届けした連載シリーズ第1回に関連する学術資料(論文)は、当サイトの『トピックス欄「1.ポールウォーキングの研究課題(その3)』にシリーズの進展に合わせ、順次掲載する予定です。
論文1:SCAN × モード切り替え ・・・・ 掲載済み
論文2:VSM × 階層的再編成 ・・・・ 未掲載
論文3:制約幾何学 × 最適面 ・・・・ 未掲載
論文4:3D 最小モデル ・・・・ 未掲載
論文5:統合論文(今回の完成稿) ・・・・ 未掲載
・『トピックス欄「1.ポールウォーキングの研究課題(その3)』へは、こちらから
・「論文1:SCAN × モード切り替え」へは、こちらから
(作成者)峯岸 瑛(みねぎし あきら)